下列叙述中不正确的是
| A.将NaAlO2溶液在蒸发皿中蒸干,最终得到的固体物质是Al(OH)3 |
| B.溶液中c(H+)>c(OH—),该溶液一定显酸性 |
| C.用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 |
| D.外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池 |
下列物质性质与应用及其对应关系均正确的是
| 选项 |
性质 |
应用 |
| A |
碳酸氢钠可与烧碱反应 |
可用碳酸氢钠作糕点膨松剂 |
| B |
AgCl难溶于稀硝酸 |
可用稀硝酸和AgNO3溶液检测Cl- |
| C |
浓硫酸具有强氧化性,而稀硫酸的氧化性较弱 |
可用浓硫酸替代稀硫酸与锌反应快速制氢气 |
| D |
碳单质性质稳定 |
可在纯铁中加入少量炭增强抗腐蚀性 |
如下图所示,各烧杯中盛有海水,铁(含杂质C)在其中被腐蚀由快到慢的顺序为
A.②①③④⑤⑥ B.⑤④③①②⑥
C.⑤④②①③⑥ D.⑤③②④①⑥
下列情况中,埋在地下的输油铁管道被腐蚀的速率最慢的是
| A.在含铁元素较多的酸性土壤中 | B.在潮湿疏松透气的土壤中 |
| C.在干燥致密不透气的土壤中 | D.在含碳粒较多、潮湿透气的中性土壤中 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是
| A.液滴中的Cl―由a区向b区迁移 |
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e- 4OH- 4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e- Cu2+ Cu2+ |
下列有关金属铁的腐蚀与防护,说法正确的是
| A.酸酸雨后易发生析氢腐蚀、炒锅存留盐液时易发生吸氧腐蚀 |
| B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀 |
| C.铁与电源正极连接可实现电化学保护 |
| D.将钢管与铜管一起堆放时可保护钢管少受腐蚀 |
以下现象与电化腐蚀无关的是( )
| A.黄铜(铜锌)制作的铜锣不易产生铜绿 | B.生铁比纯铁易生锈 |
| C.铁质器件附有铜质配件,在接触处易生铁锈 | D.银质奖牌久置后表面变暗 |
下列有关钢铁腐蚀与防护的说法正确的是( )
| A.钢管与电源正极连接,钢管可被保护 |
| B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
| C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀 |
| D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+ |
将经过酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示的装置中,下列叙述正确是( )
| A.过一段时间,Ⅱ试管中的导管内水柱上升 |
| B.Ⅰ试管中铁钉由于发生电解反应而被腐蚀 |
| C.铁钉在该试管中的腐蚀速度越来越快 |
| D.Ⅰ试管中铁钉发生反应的一个电极方程式为:2Cl—-2e—=Cl2↑ |
下列容器中盛有海水,纯铁在其中被腐蚀时,由快到慢的顺序是 ( )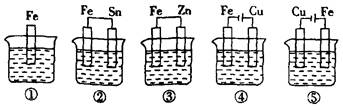
| A.⑤②①④③ | B.③②⑤①④ |
| C.⑤④②③① | D.⑤②①③④ |
下列化学实验事实及解释都正确的是
| A.向Na2S03溶液中加入硝酸酸化的BaCl2溶液,有白色沉淀出现,说明Na2S03溶液已经变质 |
| B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
C.等体积、 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性: 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性: |
D.向浓度均为0.1 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Cu(OH)2沉淀,说明 |
糕点(如月饼)包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe—3e— =Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e—= 4OH— |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
下图可设计成多种用途的电化学装置。下列分析正确的是
| A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动 |
| B.将a与电源正极相连可以保护锌片,这叫牺牲阳极的阴极保护法 |
| C.当a和b用导线连接时,铜片上发生的反应为:2H++2e →H2↑ |
| D.a和b用导线连接后,电路中通过0.02mol电子时,产生0.02mol气体 |