下列叙述错误的是()
| A. | 生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B. | 用锡焊接的铁质器件,焊接处易生锈 |
| C. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D. | 铁管上镶嵌锌块,铁管不易被腐蚀 |
下列有关说法错误的是
| A.为保护海轮的船壳,常在船壳上镶入锌块 |
| B.纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应 |
| C.已知工业合成氨气△H<0,达平衡后,升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| D.NH3(g) + HCl(g)="=" NH4Cl(s)较低温度下能自发进行,说明该反应的△H<0 |
下列叙述不正确的是
| A.金属腐蚀的本质是金属原子失去电子而被氧化 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.电解饱和食盐水制氢氧化钠,可以用铁做阴极 |
| D.氢氧燃料电池中,氢气在负极发生氧化反应 |
下图是研究铁钉腐蚀的装置图,下列说法不正确的是
| A.铁钉在两处的腐蚀速率:a < b |
| B.a、b两处铁钉中碳均正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O |
下列说法不正确的是:
| A.通过煤的干馏可获得苯、甲苯等芳香烃 |
| B.在海轮外壳装上锌块,可减缓船体的腐蚀速率 |
| C.电渗析法、离子交换法中,只有后者可以应用于海水的淡化 |
| D.我国城市推广使用清洁燃料是压缩天然气类和液化石油气类 |
下图是研究铁钉腐蚀的装置图。下列说法不正确的是
| A.ab在两处的腐蚀速率.a<b |
| B.a、b两处铁钉中的碳均为正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+ 4 H+=2H2O |
关于下列各装置图的叙述中,正确的是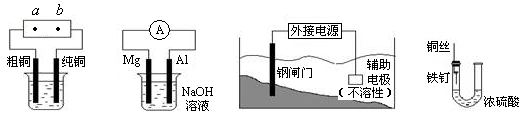
① ② ③ ④
| A.用装置①精炼铜,则a极为电源正极,电解质溶液为CuSO4溶液 |
| B.装置②中Mg为负极 |
| C.装置③中钢闸门应与外接电源的正极相连 |
| D.装置④中的铁钉被腐蚀 |
(届重庆南开中学高三二诊模拟考理综化学试卷)
下列实验装置能达到实验目的的是
| A.海水蒸馏 | B.钾在空气中的燃烧 | C.测定中和热 | D.牺牲阳极的阴极保护法 |
(届重庆南开中学高三二诊模拟考理综化学试卷)
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
下列叙述错误的是
| A.生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B.用锡焊接的铁质器件,焊接处易生锈 |
| C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D.铁管上镶嵌锌块,铁管不易被腐蚀 |
下列与金属腐蚀有关的说法正确的是
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn - MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
下列金属防腐的措施中,使用外加电流的阴极保护法的是
| A.水中的钢闸门连接电源的负极 | B.金属护拦表面涂漆 |
| C.汽车底盘喷涂高分子膜 | D.地下钢管连接镁块 |
下列与金属腐蚀有关的说法正确的是 ( )
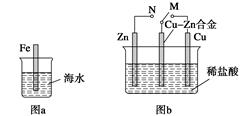
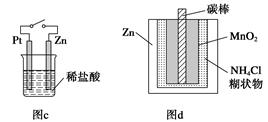
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,CuZn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,ZnMnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
以下现象与电化腐蚀无关的是
| A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B.生铁比软铁芯(几乎是纯铁)容易生锈 |
| C.铁质器件附有铜质配件,在接触处易生铁锈 |
| D.银质奖牌久置后表面变暗 |
利用如图所示装置可以模拟钢铁的电化学防护。下列说法正确的是
| A.若X为锌棒,开关K置于M处,铁极发生还原反应 |
| B.若X为碳棒,开关K置于N处,X极发生还原反应 |
| C.若X为碳棒,开关K置于N处,可加快铁的腐蚀 |
| D.若X为锌棒,开关K置于M处,可加快铁的腐蚀 |