某温度下将一定量密度为1.15g/cm3的NaCl溶液用石墨电极直流电,设NaCl恰好完全反应,且无其它反应发生,得到的溶液中氧元素的质量分数为80%。
(1)求电解后溶液中溶质与溶剂的物质的量之比;
(2)求原NaCl溶液的物质的量浓度。
用铂作电极电解500 mL含KNO3和Cu(NO3)2的混合蒲液一段时向后,在两极均生成11.2L标准状况下的气体,原溶液中Cu2+的物质的量浓度为 ( )
| A.0.5 mol/L | B.1 mol/L | C.2 mol/L | D.无法确定 |
把分别盛有熔融的KCl、MgCl2、Al2O3的三个电解槽串联,在一一定条件下通电一段时间后,析出K.Mg.Al的物质的量之比为 ( )
| A.l:2:3 | B.3:2-1 | C.6:3:1 | D.6:3:2 |
以石墨为电极,电解500 mL NaCl溶液,当两极产生气体总体积为16.8 mL时(标准状况),溶液的pH范围是 ( )
| A.5~6 | B.7~8 | C.8~10 | D.10~12 |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100gl0.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;
②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状况下的体积: ;
④电极c的质量变化是 g;
⑤电解前后个溶液的酸,碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
(1)甲烷是一重要的清洁能源、请写出以KOH溶液为电解质溶液,甲烷燃料电池的正极反应式: 。
(2)电解原理在化学工业中有广泛的应用。图中a为电解液,X和Y是两块电极板,则:
①若X和Y分别为铁和石墨,a为饱和食盐水,则电解时X电极反应式为 。
②若X、Y分别为石墨和铁,a为饱和食盐水,则电解过程中生成的白色固体露置在空气中,可观察到的现象是 。
(3)高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe、Ni、Ag、Au等四种金属杂质,可用电解法进行精炼制得高纯铜。电解完毕后,某兴趣小组欲对电解溶中的离子进行分离,他们通过查阅资料,得知相关氢氧化物在不同pH下的溶解度曲线如下图。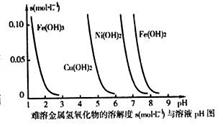
①结合右图分析,相同温度下Kap[Cu(OH)2]、Kap[Ni(OH)2]、Kap[Fe(OH)2]由大到小的顺序为 。
②分离过程中,使上述溶液的pH逐渐增加,则溶液中的Cu2+、Fe2+和Ni2+沉淀的先后顺序依次为 (填写离子符号)。
下列有关化学反应原理的应用叙述正确的是 ( )
| A.用明矾净水是因为Al2+水解生成的Al(OH)3胶粒具有很强的吸附性 |
| B.合成氨生成过程中,采用高温高压都是为了提高N2、H2转化率 |
| C.往铁钉镀铜时,用铜做阴极 |
| D.电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
下列说法正确的是
| A.强电解质溶液的导电性一定比弱电解质溶液的导电性强 |
| B.食盐溶液能导电,所以它是电解质 |
| C.SO3的水溶液可以导电,但它是不是电解质 |
| D.NaHso4无论是在水溶液里还是在熔融状态都可以电离去出Na+、H+和so42- |
用惰性电极实现电解,下列说法正确的是:
| A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变; |
| B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小; |
| C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2; |
| D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1; |
如图所示,以石墨为电极电解A的水溶液,并做下面一系列实验。试根据实验现象完成下列问题(电解质A的水溶液焰色反应呈紫色)。
(1)A的化学式为 ,E的名称为 。
(2)I和F反应的离子方程式是 。
(3)若将电解装置中的阳极换成铁棒,则在U型管底部可观察到的现象是
,阳极的电极反应式为 ,阴极的电极反应式为 ,电解的化学方程式为 。
一种新型燃料电池,它是用两根惰性金属做电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为: X极:CH4+10OH-―8e-=CO32-+7H2O Y极:4H2O+2O2+8e-=8OH-
关于此燃料电池的下列说法中错误的是
| A.X极为负极,Y极为正极 |
| B.工作一段时间后,KOH的物质的量不变 |
| C.在标准状况下通入5.6LO2完全反应,则有1.0mol电子发生转移 |
D.该电池工作时甲烷 一极附近溶液的pH降低 一极附近溶液的pH降低 |
用惰性电极电解一定质量的某浓度的NaCl溶液,一段时间后停止电解,此时若加入100g 36.5%的浓盐酸,所得溶液正好与原溶液完全相同,则下列说法正确的是
| A.电解过程中,两极所得到的气体,在相同的条件下体积相等 |
| B.电解过程中,在相同的条件下,阳极所得到的气体的体积比阴极的大 |
| C.电解过程中转移电子的物质的量约为8mol |
| D.原某浓度的NaCl溶液中溶有117g NaCl |
现有Cu2 +、Cl―、Na+、SO42―、Zn2+两两组成的电解质溶液若干种,可选用铜电极、铂电极、锌电极进行电解实验。
+、Cl―、Na+、SO42―、Zn2+两两组成的电解质溶液若干种,可选用铜电极、铂电极、锌电极进行电解实验。
(1)以铜为阳极电解_________或____________溶液,均可得到氢氧化物沉淀。
(2)要使电解过程中溶质的组成和质量不变,而溶液浓度增大,又无浑浊,应以
__________为阳极电解_____________溶液,化学方程式为_______________________。
(3)要使电解过程中溶液浓度改变,而溶剂 质量不变,应以铂电极为阳极电解___________溶液,或以_________为阳极电解________溶液,前者反应的化学方程式是_________________________。
质量不变,应以铂电极为阳极电解___________溶液,或以_________为阳极电解________溶液,前者反应的化学方程式是_________________________。
(4)使反应Cu+2H2O==Cu(OH)2 ↓+H2 ↑ 得以进行而不发生其它反应,可选用______________为阳极电解__________或____________溶液
(5)以铜为阳极电解ZnSO4溶液,阴极上一般有___________逸出,在________极区首先会有__________色沉淀,电解时间较长时,会有______色沉淀出现。
(1)如右图所示,用两根质量相等的银棒作电极电解CuCl2溶液,电解一段时间后,①现象为 ,
②a、b两极比较, 极重,写出a极上发生的反应 。
(2)下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g10.00%的K2SO4溶液,电极均为石墨电极。
I.接通电源,经过一段时间后,测得丙中K2SO4的浓度变为10.47%,乙中c电极质量增加。据此回答下列问题。
①电源的N端为 极;
②电极b上发生的电极反应为: 。
③电极b上生成的气体在标准状况下的体积为: L。
④电极c的质量变化是: g。
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液: , 。
乙溶液: , 。
丙溶液: , 。
II.如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
, 。