如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16 g,乙池中某电极上析出0.64 g某金属,下列说法正确的是
| A.甲池b极上析出金属银,乙池c极上析出某金属 |
| B.甲池a极上析出金属银,乙池d极上析出某金属 |
| C.某盐溶液可能是CuSO4溶液 |
| D.某盐溶液可能是Mg(NO3)2溶液 |
在外界提供相同电量的条件下,Cu2+或Ag+分别按Cu2++2e-="Cu" 或Ag++e-=Ag在电极上放电,若析出铜的质量为1.92g,则析出银的质量为 ( )
| A.12.96g | B.3.24g | C.6.48g | D.1.62g |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )
| A.a为阳极、b为阴极 | B.a为负极、b为正极 |
| C.电解过程中,氯离子浓度不变 | D.电解过程中,d电极质量增加 |
如图装置,U型管中盛有Fe(OH)3胶体,以两个碳棒为电极进行电解,一段时间后,下列叙述正确的是
| A.x是阳极,y是阴极 |
| B.x极附近颜色变深,y极近颜色变浅 |
| C.x是阴极,y极附近颜色加深 |
| D.y是阴极,x极附近颜色加深 |
下列叙述正确的是
| A.在电解池的阴极和原电池的负极上都发生氧化反应 |
| B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C.用惰性电极电解KOH溶液,阴、阳两极产物的物质的量之比为1:2 |
| D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
以惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol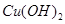 ,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
| A.0.1mol | B.0.2mol | C.0.3mol | D.0.4mol |
用铂电极电解100mL HNO3 与 AgNO3的混合液,通电一段时间后,两极均收集到
2.24 L气体(标准状况),则原混合液中Ag+的物质的量浓度为
A.1mol·L-1 B.2 mol·L-1 C.2.5 mol·L-1 D.3 mol·L-1
用惰性电极电解CuSO4溶液一段时间后,欲使溶液恰好恢复至电解前情况,可加入的物质是( )
| A.CuSO4 | B.Cu(OH)2 | C.Cu | D.CuO |
如图所示,各烧杯中盛有海水,铁(含杂质C)在其中被腐蚀由快到慢的顺序为( )
A.⑤④②①③⑥ B.⑤④③①②⑥ C.②①③④⑤⑥ D.⑤③②④①⑥
中央电视台报道,一种名叫“排毒基强离子排毒仪”的产品正在市场热销。向排毒盆内倒入了纯净的温水,双脚放入盆中,启动电源开关,加入了适量精盐。过一段时间,盆中开始出现绿色、红褐色的絮状物。下列说法正确的是 ( )
| A.此“排毒基强离子排毒仪”一定是用惰性电极制成的 |
| B.绿色、红褐色的絮状物是氢氧化亚铁、氢氧化铁形成的混合物 |
| C.绿色、红褐色的絮状物就是从脚底排出的体内毒素 |
| D.加一些精盐的主要目的只是起到消炎杀菌的作用 |
右图,是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列判断正确的是( )
| A.a为负极、b为正极 |
| B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下左图所示。下列说法中,正确的是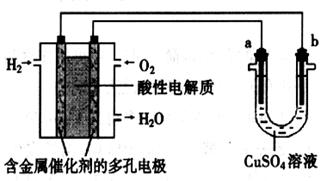
| A.若a极是铜,b极为铁时,当电池消耗1.6g O2,b极上析出6.4g铜 |
| B.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| C.若a极是粗铜,b极是纯铜时,a极减少的质量等于b极上析出铜的质量。 |
| D.若a、b两极均是石墨时,b极反应为4OH- - 4e-=O2↑+ 2H2O |
下列叙述正确的是
| A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过 |
| B.在铁上镀锌时,锌棒作阳极,且电解液硫酸锌的浓度是不变的 |
| C.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1: 2 |
| D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
如右图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色 “彩虹”,从右到左颜色的次序是
| A.蓝、紫、红 | B.红、蓝、紫 |
| C.红、紫、蓝 | D.紫、红、蓝 |