Ⅰ.A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
(1)推断B元素在元素周期表中的位置_______________________。
(2)A与D形成的18电子的化合物与FD2化合生成一种强酸,其化学方程式为_____________。
(3)用电子式表示化合物E2F的形成过程_______________________。
(4)下图为某新型发电装置示意图,其负极电极反应为_______________________。

(5)在101kPa、25℃下,16g液态C2A4在D2中完全燃烧生成气体C2,放出312kJ热量,则C2A4和D2反应的热化学方程式为_______________________。
Ⅱ.A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去)。
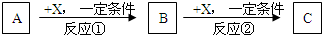
试回答:
(1)若X是强氧化性单质,则A不可能是___________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的 化 学式为___________。
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为___________。
X、Y、Z、U、V是元素周期表前四周期中的五种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
地壳中含量最多的金属,其氧化物可用作耐火材料 |
| Y |
单质在常温常压下为黄绿色气体 |
| Z |
常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
| U |
常温下单质遇浓硫酸钝化,其一种核素的质量数为56,中子数为30 |
| V |
属短周期元素,原子的最外层电子数是内层电子数的2/5 |
请回答下列问题:
(1)元素X位于周期表中第 周期第 族,其离子结构示意图为 。
(2)上述元素中最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)在碱性条件下,Y的单质可与UO2-反应制备一种可用于净水的盐UO42-,该反应的离子方程式是 。
(4)我国首创的海洋电池被大规模用于海洋灯塔。该电池是以X板为负极,铂网为正极,海水为电解质溶液,电池总反应为:4X+3O2+6H2O=4X(OH)3。该电池正极反应为 。
(5)已知25℃时,Ksp[U(OH)3]=2.63×10-39,则该温度下反应U(OH)3+3H+ U3++3H2O的平衡常数K= 。
U3++3H2O的平衡常数K= 。