下列是构成原电池的实验方案, 请按要求回答下列问题:
(1)电解质溶液为0.5mol·L-1硫酸溶液,电极为用砂纸打磨过的镁片和铝片,设计成原电池,则铝片为
极(填“正”或“负”),正极电极反应式为 ;若将电解质溶液改为0.5mol·L-1氢氧化钠溶液,则被氧化的是 (填“镁片”或“铝片”),该原电池总反应的离子方程式为:
(2)以“Fe+2Fe3+===3Fe2+ ”反应为原理设计原电池,请在以下该原电池装置图括号中写出电极材料及电解质溶液。
(1)已知:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1;
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH2,则ΔH1 ΔH2
(2)在298K、100kPa时,已知:
2H2(g)+O2(g)==2H2O(g) ΔH1
2HCl(g)==Cl2(g)+H2(g) ΔH2
4HCl(g)+O2(g)==2Cl2(g)+2H2O(g) ΔH3
则ΔH3与ΔH1和ΔH2的关系是:ΔH3=
(3)消除氮氧化物的污染对环境至关重要,用CH4催化还原NOx可以消除氮氧化物的污染。已知一定条件下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
则该条件下,用CH4还原NO2至N2的热化学方程式为:
(4)乙烯是石油裂解气的主要成分之一, 25℃、101kPa时,1g乙烯燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为 __;利用该反应设计为燃料电池中,通入乙烯的电极为电池的________(填“正极”或“负极”)。
(1)请用“>”、“<”或“=”填写下列空格:
①已知:Zn(s)+CuSO4(aq)==ZnSO4(aq)+Cu(s)ΔH="-216" kJ·mol-1,则E反应物 E生成物
②由A、B两金属作电极,硫酸溶液作电解质溶液,形成原电池,电流由A极经外电路流向B极,则金属活泼性A B
③镀层破损后铁的腐蚀速度比较:镀锌铁管 镀锡铁管
(2)用“增大”、“减小”或“不变”填写下列空格:
④以石墨为电极电解Na2SO4溶液时,电解过程中阳极区溶液的pH
⑤某温度下,可逆反应A(s)+ B(g) 2C(g);△H<0,平衡常数为K。其它条件不变时,温度升高,平衡常数K
2C(g);△H<0,平衡常数为K。其它条件不变时,温度升高,平衡常数K
反应Cu(s)+2Ag+(aq) Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
| A.KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B.Ag作负极,Cu作正极 |
| C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大 |
| D.取出盐桥后,电流计的指针依然发生偏转 |
把A、B、C、D 4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若A、B相连时,A为负极;C、D相连时,D上产生大量气泡;A、C相连时,电流由C经导线流向A;B、D相连时,电子由D经导线流向B,则此4种金属的活动性由强到弱的顺序为
A、A>B>C>D B、A>C>D>B C、C>A>B>D D、B>A>C>D
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-===ZnO+H2O;Ag2O+H2O+2e-===2Ag+2OH-。总反应式为:Ag2O+Zn===2Ag+ZnO,下列说法正确的是
| A.Zn为正极,Ag2O为负极 |
| B.Zn为负极,Ag2O为正极 |
| C.原电池工作时,正极区溶液pH值减小 |
| D.原电池工作时,负极区溶液pH值增大 |
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极。则四种金属的活动性顺序由大到小排列为
A.A>B>C>D B.A>C>B>D C.A>C>D>B D.B>D>C>A
根据下列事实,判断离子的氧化性顺序为①A+B2+===A2++B②D+2H2O===D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-=B2+
A.D2+>A2+>B2+>E2+ B.D2+> E2+ >B2+>A2+
C.E2+>B2+>A2+>D2+ D.A2+>B2+>D2+>E2+
某学习小组为研究电化学原理,设计下图装置。下列叙述正确的是
| A.K与M、N均断开,一段时间后电解质溶液质量变大 |
| B.K分别与M、N相连时,铁均受到保护 |
| C.K与M相连时,每转移1mol电子Fe表面生成32gCu |
| D.K与N相连时, 碳棒上产生使湿润的淀粉碘化钾试纸变蓝的气体 |
有A、B、C、D四种短周期主族元素,其原子序数依次增大。A、B可形成A2B和A2B2两种共价化合物,B、C同主族且可形成CB2和CB3两种化合物。完成下列问题。
(1)C的名称为________
(2)写出表示非金属性C<D的化学方程式(任一个):________ 。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中,溶液由黄色逐渐变为浅绿色,该反应的离子方程式为______________。
(4)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出负极反应式。
负极反应式:__________________________________________________________。
分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
(1)以下叙述中,正确的是__________。
| A.甲中锌片是负极,乙中铜片是正极 |
| B.两烧杯中铜片表面均有气泡产生 |
| C.两烧杯中溶液pH均增大 |
| D.产生气泡的速度甲中比乙中慢 |
E.乙的外电路中电流方向Zn→Cu
(2)变化过程中能量转化的形式主要是:甲为__________;乙为__________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是__________。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式:_____________
请按要求回答下列问题。
(1)根据下图回答①②。
①打开K2,闭合K1。A极电极反应式为_________________,B极的现象____________。
②B极重新换根碳棒,再打开K1,闭合K2。
B极电极反应式_______________________________。
装置发生的总反应化学方程式______________。实验完成后,锌电极增重a g,则阳极产生标准状况下的气体体积_____ ___L。
(2)改变两电极的电极材料,利用该装置要实现Cu+H2SO4== CuSO4+H2↑反应的发生,应打开____闭合_____,其电解质溶液需用 ,B电极材料是用 ,A电极反应式为 。
把a、b、c、d 4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时, d上产生大量气泡;a、c相连时,电流由c经导线流向a;b、d相连时,电子由d经导线流向b,则此4种金属的活动性由强到弱的顺序为
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>a>c>d |
阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解液为KOH,反应保持在较高温度,使H2O蒸发,下列叙述正确的是
| A.此电池工作时会发出蓝色火焰 |
| B.燃料电池具有能量转化率高、可持续使用的优点 |
| C.该电池的负极电极反应式为:2H2+4e-=4H+; |
| D.该电池的正极电极反应式为:O2+2H2O+4e -=4OH- |
A、B、C、X是中学化学常见物质,它们在一定条件下具有如下转化关系:
A + X → B + C + H2O
(1)若X是淀粉水解的最终产物,B为砖红色难溶于水的氧化物。
①X的化学式为 。
②A溶于硝酸的离子方程式为 。
③将淀粉水解液中和后,与A的悬浊液(含NaOH)共热至沸腾,产生砖红色沉淀则证明淀粉已经水解。若要进一步探究淀粉是否完全水解,还需用到的试剂是 。
(2)若A是由M+和R-构成的盐,X为二元强碱,B为气体。
①B与氧气一定条件下可以发生置换反应,当生成18g液态水时,放出能量Q kJ,该反应的热化学方程式为 ;若将该反应设计成燃料电池(以硫酸溶液为电解质溶液),其负极反应式为 。
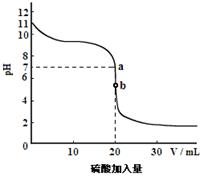
②室温时,20mL 0.10mol·L-1的B溶液用0.050mol·L-1的硫酸溶液滴定,所得滴定曲线如图所示。曲线上a点,c(M+) c(SO42-)(填“>”、“<”或“=”)。曲线上b点,溶液中c(H+)≈ (只保留一位有效数字)。