下列说法不正确的是
| A.探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合 |
| B.用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值 |
| C.H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
| D.欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸 |
在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度 ②升高温度 ③增大压强 ④移去生成物 ⑤加入催化剂
| A.①③⑤ | B.②⑤ | C.②③⑤ | D.①③④ |
工业合成氨是人工固氮方法之一。
I.已知下列物质的键能:

则N2(g)+3H2(g)=2NH3(g) △H=_____________。
Ⅱ.恒温下,将一定量N2、H2置于10L的容器中发生反应,反应过程中各物质浓度随时间变化如下图。
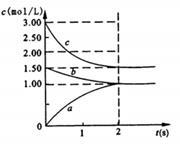
(1)图中0~2s内的反应速率v(H2)= ;该温度下平衡常数的计算表达式为__________。
(2)该反应达到平衡的标志为 (填序号)。
| A.混合气体的平均相对分子质量不变 |
| B.物质的量浓度比等于系数比 |
| C.容器内温度不变 |
| D.断裂1moIH-H键同时断裂2molN-H键 |
(3)若其它条件不变,将恒容条件变为恒压,则平衡时c(N2) (填“增大”、“减小”、“不变’’或“不能确定”)。
(4)哈伯研究所因证实N2、H2在固体催化剂(Fe)表面吸附和解吸以合成氨的过程而获诺贝尔奖。若用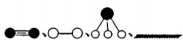 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:

①吸附后,能量状态最低的是 (填字母序号)。
②由上述原理,在铁表面进行NH3的分解实验,发现分解速率与浓度关系如图。从吸附和解吸过程分析,c0前速率增加的原因可能是 ;c0后速率降低的原因可能是 。

在C(s)+CO2(g)  2CO(g)反应可使反应速率增大的措施是
2CO(g)反应可使反应速率增大的措施是
①增大压强 ②增加碳的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2
| A.①③⑤ | B.②④ | C.①③ | D.③⑤ |
下列图示与对应的叙述相符的是
A.图I表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H =" -" 241.8 kJ.mol-1
B.图Ⅱ表示某可逆反应正、逆反应速率随温度的变化,则该反应的正反应是放热反应
C.图Ⅲ表示0.1 mol MgCl2.6H2O在空气中充分加热时固体质量随时间的变化
D.图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
| A.NaOH(固体) | B.KNO3 |
| C.HCl | D.CH3COONa(固体) |
下列有关说法正确的是
| A.实验室制氢气,为了加快反应速率,可向稀 H2SO4中滴加少量 Cu(NO3)2溶液 |
B.N2(g)+3H2(g)  2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 |
C.吸热反应“TiO2(s)+2Cl2(g)  TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的ΔS<0 TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的ΔS<0 |
| D.为处理锅炉水垢中的 CaSO4,可先用饱和 Na2CO3溶液浸泡,再加盐酸溶解 |
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为:2Al2O3(s)+6Cl2(g) 4AlCl3(g)+3O2(g)△H>0.下列分析错误的是
4AlCl3(g)+3O2(g)△H>0.下列分析错误的是
| A.增大反应体系的压强,反应速率可能加快 |
| B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 |
| C.电解熔融的Al2O3和AlCl3溶液均能得到单质铝 |
| D.将AlCl3•6H2O在氯化氢气流中加热,也可制得无水氯化铝 |
少量铁片与l00mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KNO3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)
⑧改用10mL 0.1mol/L盐酸.
| A.①⑥⑦ | B.③⑤⑧ |
| C.③⑦⑧ | D.③④⑥⑦⑧ |
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+ 3B2(g)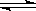 2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
A.若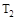 > >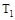 ,则正反应是放热反应 ,则正反应是放热反应 |
B.达到平衡时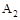 的转化率大小为:b>a>c 的转化率大小为:b>a>c |
C.若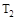 > >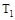 ,达到平衡时b、d点的反应速率为 ,达到平衡时b、d点的反应速率为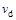 > >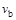 |
D.在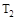 和 和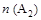 不变时达到平衡, 不变时达到平衡, 的物质的量大小为:c>b>a 的物质的量大小为:c>b>a |
在密闭容器中进行下列反应:M (g)+N (g)  R (g)+2 L此反应符合下面图像。下列叙述正确的是
R (g)+2 L此反应符合下面图像。下列叙述正确的是
| A.正反应放热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应吸热,L是气体 |
| D.正反应放热,L是液体 |
下列说法中有明显错误的是
| A.对有气体参加的化学反应,增大压强体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 |
| B.升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率 |
I、某学生实验小组用50mL0.50mol•L—1的盐酸与50mL0.50mol•L—1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
(1)图中装置缺少的一种仪器,该仪器名称为 。

(2)将反应混合液的 温度记为反应的终止温度。
(3)下列说法正确的是
| A.小烧杯内残留有水,会使测得的反应热数值偏小 |
| B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验 |
| C.烧杯间填满碎纸条的作用是固定小烧杯 |
| D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅 |
II、某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 |
反应物 |
催化剂 |
| ① |
10mL2% H2O2溶液 |
无 |
| ② |
10mL5% H2O2溶液 |
无 |
| ③ |
10mL5% H2O2溶液 |
1mL0.1mol·L-1FeCl3溶液 |
| ④ |
10mL5% H2O2溶液+少量HCl溶液 |
1mL0.1mol·L-1FeCl3溶液 |
| ⑤ |
10mL5% H2O2溶液+少量NaOH溶液 |
1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是__________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。

分析上图能够得出的实验结论是_______________________。