一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
| A.NaOH(固体) | B.KNO3 |
| C.HCl | D.CH3COONa(固体) |
下列有关说法正确的是
| A.实验室制氢气,为了加快反应速率,可向稀 H2SO4中滴加少量 Cu(NO3)2溶液 |
B.N2(g)+3H2(g)  2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 |
C.吸热反应“TiO2(s)+2Cl2(g)  TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的ΔS<0 TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的ΔS<0 |
| D.为处理锅炉水垢中的 CaSO4,可先用饱和 Na2CO3溶液浸泡,再加盐酸溶解 |
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为:2Al2O3(s)+6Cl2(g) 4AlCl3(g)+3O2(g)△H>0.下列分析错误的是
4AlCl3(g)+3O2(g)△H>0.下列分析错误的是
| A.增大反应体系的压强,反应速率可能加快 |
| B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 |
| C.电解熔融的Al2O3和AlCl3溶液均能得到单质铝 |
| D.将AlCl3•6H2O在氯化氢气流中加热,也可制得无水氯化铝 |
少量铁片与l00mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KNO3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)
⑧改用10mL 0.1mol/L盐酸.
| A.①⑥⑦ | B.③⑤⑧ |
| C.③⑦⑧ | D.③④⑥⑦⑧ |
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+ 3B2(g)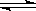 2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
A.若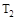 > >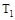 ,则正反应是放热反应 ,则正反应是放热反应 |
B.达到平衡时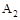 的转化率大小为:b>a>c 的转化率大小为:b>a>c |
C.若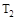 > >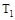 ,达到平衡时b、d点的反应速率为 ,达到平衡时b、d点的反应速率为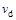 > >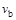 |
D.在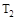 和 和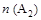 不变时达到平衡, 不变时达到平衡,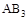 的物质的量大小为:c>b>a 的物质的量大小为:c>b>a |
在密闭容器中进行下列反应:M (g)+N (g)  R (g)+2 L此反应符合下面图像。下列叙述正确的是
R (g)+2 L此反应符合下面图像。下列叙述正确的是
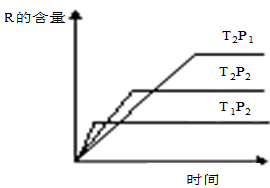
| A.正反应放热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应吸热,L是气体 |
| D.正反应放热,L是液体 |
下列说法中有明显错误的是
| A.对有气体参加的化学反应,增大压强体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 |
| B.升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率 |
反应3Fe(s)+4H2O(g)⇌Fe3O4(s)+4H2(g)在一体积可调的密闭容中进行,下列条件的改变对其反应速率几乎无影响的是
| A.增加Fe的表面积 |
| B.保持体积不变,充入Ne使体系压强增大 |
| C.将容器的体积缩小一半 |
| D.保持总压强不变,充入Ne使容器的体积增大 |
如图所示曲线表示其他条件一定时,反应:2NO+O2 2NO2 ΔH<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 ΔH<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
| A.a点 | B.b点 |
| C.c点 | D.d点 |
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡: CO(g)+H2S(g) COS(g)+H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
| A.升高温度,H2S浓度增加,表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大 |
| C.反应前H2S物质的量为7mol |
| D.CO的平衡转化率为80% |
下列说法不正确的是
| A.增大压强,活化分子百分数不变,化学反应速率增大 |
| B.升高温度,活化分子百分数增大,化学反应速率增大 |
| C.加入反应物,活化分子百分数增大,化学反应速率增大 |
| D.使用催化剂,活化分子百分数增大,化学反应速率增大 |
为探究足量锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
| A.加入NH4HSO4固体,v(H2)不变,生成H2量不变 |
| B.加入少量水,v(H2)减小,生成H2量减少 |
| C.加入CH3COONa固体,v(H2)减小,生成H2量不变 |
| D.滴加少量CuSO4溶液,v(H2)增大,生成H2量减少 |
已知反应:2NO2 (红棕色)  N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,下右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,下右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是

| A.b点的操作是拉伸注射器 |
| B.d 点:v(正) < v(逆) |
| C.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| D.若不忽略体系温度变化,且没有能量损失,则温度关系:T(b)>T(c) |
在恒容密闭容器中加入一定量的反应物后存在下列平衡:
CO(g)+H2O(g) CO2(g)+H2(g),平衡时CO2物质的量浓度与温度的关系如图所示,下列说法正确的是
CO2(g)+H2(g),平衡时CO2物质的量浓度与温度的关系如图所示,下列说法正确的是
A.该反应的DH <0
B.在T2时,D点的反应速率:ν(正)<(逆)
C.A、C两点相比,混合气体的平均相对分子质量:M(A) < M(C)
D.若T1、T2时的平衡常数分别为K1、K2,则K1>K2