设体积的单位为L。用V体积水制得物质的量浓度为a(密度为p),需要标况下氨气的体积为________________________.
析:
某化合物的化学式可表示为 (x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用
(x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用 溶液滴定(生成
溶液滴定(生成 沉淀),共消耗24.0mL 0.100mol/L的
沉淀),共消耗24.0mL 0.100mol/L的 溶液。在另一份试样中加入过量
溶液。在另一份试样中加入过量 溶液并加热,用足量盐酸吸收逸出的
溶液并加热,用足量盐酸吸收逸出的 。吸收
。吸收 共消耗24.0mL 0.200mol/L
共消耗24.0mL 0.200mol/L  溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)
溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)
将0.04molKMnO4固体加热,一段时间后,收集到amol气体,此时KMnO4的分解率为x,在反应后的残留固体中加入足量的浓盐酸,又收集到bmol气体(设Mn元素全部以Mn2+存在于溶液中)。试填写:
(1)a+b=__________(用x表示)。
(2)当x=__________时,a+b取最小值,且最小值为___________。
(3)当a+b=0.09时,加热后所得残留固体的质量为___________g。
将6.5 g锌放入足量的稀硫酸中充分反应,得到80 mL密度为1.25 g/mL的溶液。试计算所得溶液中硫酸锌的物质的量浓度和质量分数各是多少?
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧: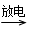
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为(保留一位小数)。
(2)将8氧气通过放电管后,恢复到原状况,得到气体6.5
,其中臭氧为
。
(3)实验室将氧气和臭氧的混合气体0.896(标准状况)通入盛有20.0
铜粉的反应器中,充分加热后,粉末的质量变为21.6
。则原混合气中臭氧的体积分数为。
如图所示支管中,左管中放入KMnO4固体,右管中放入一小块钠,再向两管均加入适量8mol·L-1的盐酸,半分钟后,盖以橡胶塞并将此支管固定在铁架台上。用一照相机对准此支管,按快门,闪光灯闪亮。请回答:
(1)“照像”之前,左管中反应的离子方程式__________________________。
(2)“照像”时,灯光闪亮,支管随之出现的现象为______________________,
化学方程式为_______________________________________。
在Al2(SO4)3和MgSO4组成的混合物中,Al3+与Mg2+的物质的量之比为2∶3,则在含有2 mol
SO42-的混合物中,MgSO4的质量是多少克?
有CO与CO2的混合气体共33.6 L,其密度为1.726 g/L,已知混合气体共有9.03×1023个分子,则该混合气体的平均摩尔质量是多少?CO与CO2的分子个数比是多少?
与171 g Al2(SO4)3中所含的SO42-数目相同的Na2SO4的质量是多少?将171 g Al2(SO4)3和142 g Na2SO4混合,其混合物的平均摩尔质量是多少?
现有H2SO4和Na2SO4混合溶液200 mL,其中硫酸的物质的量浓度为1 mol·L-1,硫酸钠的物质的量浓度为0.5 mol·L-1。若要使硫酸和硫酸钠的物质的量浓度分别为2 mol·L-1和0.2 mol·L-1,应加入质量分数为55.8%的硫酸溶液(ρ="1.35" g·mL-1)多少毫升后再加蒸馏水配制?
化合物KxFe(C2O4)y·zH2O是一种重要的光化学试剂,其中铁为+3价。分别称取该样品0.491g两份,其中一份在110℃干燥脱水,至质量恒定为0.437g。另一份置于锥形瓶中,加入足量的3mol/LH2SO4和适量的蒸馏水,加热到75℃,趁热加入0.0500mol/L KMnO4溶液24.0mL,恰好完全反应;再向溶液中加入适量的某种还原剂,将Fe3+完全转化为Fe2+,该溶液中Fe2+刚好与4.0mL 0.0500mol/L KMnO4溶液完全反应。通过计算,分别求:
(1)0.491g样品中结晶水的物质的量。
(2)化合物中草酸根的质量分数。
(3)化合物的化学式。
已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
现有一含少量SiO2杂质的石灰石样品,某实验小组同学为准确测定该样品的纯度,他们取用2.0g样品于烧杯中,把25.00mL某浓度的盐酸分成5等份,准备分别加入烧杯中进行反应,他们将前4次实验的结果记录如下:
| 次序 |
盐酸 |
剩余固体 |
| 1 |
先加入5.00mL |
1.32g |
| 2 |
再加入5.00mL |
0.64g |
| 3 |
再加入5.00mL |
0.2g |
| 4 |
再加入5.00mL |
0.2g |
(1)该实验小组同学是否还需要将第5份盐酸加入烧杯? ;
(2)原样品的纯度(CaCO3的质量分数)是______________。
(3)求该实验小组同学所用盐酸的物质的量浓度。(要求写出计算过程)