以NA表示阿伏加德罗常数的值,下列说法错误的是
| A.18g冰(图1)中含O—H键数目为2NA |
| B.28g晶体硅(图2)中含有Si—Si键数目为2NA |
| C.44g干冰(图3)中含有NA个晶胞结构单元 |
| D.石墨烯(图4)是碳原子单层片状新材料,12g石墨烯中含C—C键数目为1.5NA |
两种硫酸溶液,一种物质的量浓度为C1 mol/L,密度为ρ1 g/cm3,另一种物质的量浓度为C2 mol/L,密度为ρ2 g/cm3,当它们等体积混合后,溶液的密度为ρ3 g/cm3,则混合溶液的物质的量浓度为
( )
A. |
B. |
C. |
D.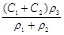 |
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/ml,质量分数为W,物质的量浓度为c mol/L,则下列关系中不正确的是 ( )
| A.W="17c/" (1000ρ) | B.ρ=(17V+22400)/(22.4+22.4V) |
| C.W="17V/(17V+22400)" | D.c=1000Vρ/(17V+22400) |
标准状况下,将VL A气体(摩尔质量为Mg/mol)溶于100克水中,所得溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为
A. |
B. |
C. |
D.1000VρM/(MV+2240) |
以下有关物质的量浓度的叙述正确的是
| A.等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为1:2:3 |
| B.150 mL 1mol·L-1的氯化钾溶液中的c(Cl-)与50 mL 1 mol·L-1的氯化铝溶液中的c(Cl-)相等 |
C.20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0 mol·L-1,则此溶液中KCl的质量分数为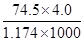 ×100% ×100% |
| D.20℃时,100 g水可溶解34.2g KCl,此时KCl饱和溶液的质量分数为34.2% |
向三份同浓度的25mL盐酸中分别加入质量不等的NaHCO3、KHCO3的混合物,测得产生气体的体积如下表所示(不考虑气体溶解)
| 编号 |
1 |
2 |
3 |
| m(混合物)/g |
4.6 |
7.2 |
7.9 |
| V(CO2)(标准状况)/L |
1.12 |
1.68 |
1.68 |
下列分析推理正确的是
A.根据实验1中的数据可以计算出盐酸的浓度
B.混合物中NaHCO3的质量分数约为45.7%
C.根据第2、3组数据可以分析出第2组中的混合物完全反应
D.盐酸的物质的量浓度为1.5mol.L-1
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
| A.abcd | B.bcd | C.cba | D.abc |
下列溶液中物质的量浓度肯定是1mol/L的是( )
| A.将40gNaOH固体溶解于1L水中 |
| B.将22.4L氯化氢气体溶于水配成1L溶液 |
| C.将1L10mol/L浓盐酸与10L水混合 |
| D.10gNaOH固体溶解在水中配成250mL溶液 |
NA代表阿伏加德罗常数的值,下列说法正确的是
| A.2.8g铁与0.05mol Cl2充分反应,转移0.15NA电子 |
| B.27g Al与足量NaOH溶液反应生成 33.6L H2 |
| C.14g由乙烯(C2H4)和丙烯(C3H6)组成的混合物中含有原子的数目为3NA |
| D.0.1mol Na2O2与足量二氧化碳反应转移0.2NA个电子 |
若NA为阿伏加德罗常数的值,下列说法正确的是
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| D.5.6gFe与0.1mol Cl2完全反应,反应中转移的电子数为0.3NA |
用NA表示阿伏加德罗常数,下列有关说法正确的是
| A.在常温常压下,11.2LN2含有的分子数小于0.5NA |
| B.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| C.将1 L2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D.46g NO2和N2O4混合气体所含氧原子数有可能为3NA |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.在常温常压下,11.2 L Cl2含有的分子数为0.5NA |
| B.在常温常压下,17 g NH3所含的原子数为4NA |
| C.标准状况下,11.2 L CCl4所含的分子数为0.5NA |
| D.56g金属铁与足量的氯气反应时,失去的电子数为2NA |
NA为阿伏加德罗常数的值。下列说法正确的是
| A.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
| B.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
| C.过氧化钠与CO2反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.在标准状况下,2.24LH2O中原子数为0.3NA |
| B.0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA |
| C.16g O2和O3的混合气体中含NA个O原子 |
| D.64克铜与足量的硫反应生成硫化铜,理论上会转移2NA个电子 |