下列说法正确的是
| A.1molO2的质量是32g.mol—1 |
| B.H2的摩尔质量是2g |
| C.1molH+的质量是1g |
| D.对原子而言,摩尔质量就是相对原子质量 |
在t℃时,将a gNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg/cm3,质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是( )
| A.溶质的质量分数w=(1000a/17V)100% |
| B.溶质的物质的量浓度c=1000a/17V (mol/L) |
| C.溶液中c(OH-)=b/V (mol/L) |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
下列关于NH4+与CH4的相关数目比较前者大于后者的是
| A.电子数 | B.化学键数 | C.质子数 | D.原子数 |
在标准状况下充满HCl的烧瓶做完喷泉实验后得到稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在__________式滴定管内,若用甲基橙作指示剂,达到滴定终点时,溶液从_________色变为____________色;
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第_____________种(填序号);
①2.500 mol/L ②0.25 mol/L ③0.025mol/L
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO 3)表示,滴定时实验数据列表如下:
| 实验编号 |
待测盐酸体积(mL) |
滴入Na2CO3溶液体积(mL) |
| 1 |
20.00 |
18.80 |
| 2 |
20.00 |
16. 95 |
| 3 |
20.00 |
17. 05 |
根据以上数据计算时应带入的Na2CO3溶液体积_______________求这种待测盐酸的物质的量浓度(用数据和符号列式即可):c(HCl)=_________________。
氢气是一种清洁的可再生能源。上海最新研发的“超越”3号氢燃料电池轿车,每行驶100km仅耗氢气1kg左右,同时消耗氧气约为
| A.250mol | B.500mol | C.8kg | D.16kg |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
如右图。反应中镁和铝的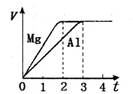
| A.物质的量之比为3:2 | B.质量之比为2:3 |
| C.摩尔质量之比为2:3 | D.反应速率之比为3:2 |
下列叙述正确的是 ( )
| A.1 mol任何气体的气体摩尔体积都约为22.4 L/mol |
| B.常温常压下,11.2LO3中所含氧原子个数等于1.5NA |
| C.标准状况下,1mol CCl4所占的体积约为22.4L |
| D.同温、同压下,相同体积的一氧化碳和二氧化碳的质量比为7:11 |
设NA 表示阿伏加德罗常数,数值约为6.02×1023。下列说法正确的是
| A.1 L 0.1mol·L-1的NaHCO3溶液中含有阳离子的物质的量为0.2mol |
| B.0.1 mol水蒸气在标准状况下体积为2.24 L |
| C.在25℃,1.01×105 Pa时,11.2 L氧气所含的氧原子数目为6.02×1023 |
| D.标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24 L |
下列物理量与所对应的单位不正确的是
| A.n:mol | B.M:g.mol-1 | C.Vm,:L.mol-l | D.NA:个 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A.标准状况下,11.2L的戊烷所含的分子数为0.5×6.02×1023 mol-1 |
| B.28g乙烯所含共用电子对数目为4×6.02×1023 mol-1 |
| C.1mol 苯中含有碳碳双键的数目为3×6.02×1023 mol-1 |
| D.2.8g聚乙烯中含有的碳原子数为0.2×6.02×1023 mol-1 |
用水处理金属钠与碳化钙的混合物,有气体放出,此气体在催化剂作用下恰好完全反应,生成另一种气体A.气体A完全燃烧时,需要3.5倍体积的氧气,则金属钠与碳化钙的物质的量之比是
A.2:1 B.1:2 C.4:1 D.1:4
NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,3.36L氧气与3.2g硫反应,生成SO2分子数为0.1NA |
| B.1L0.1mol∙L-1氨水中NH3∙H2O分子数为0.1NA |
| C.标准状况下,1.12LCl2发生反应转移的电子数一定为0.1NA |
| D.10g46%酒精(C2H5OH)中含氧原子总数为0.1NA |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.过氧化钠与水反应时,生成22.4L氧气转移的电子数为2 NA |
| B.18g D2O中含有的电子数和中子数均为10 NA |
| C.密闭容器中2mol NO与1mol O2充分反应,产物的分子数为2 NA |
| D.1mol Na与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去 NA个电子 |