一定温度下, 向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2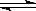 2NO+O2,此反应达到平衡的标志是
2NO+O2,此反应达到平衡的标志是
| A.单位时间内生成2nmolNO同时生成2nmolNO2 |
| B.混合气体中NO2、NO和O2的物质的量之比为2:2:1 |
| C.单位时间内生成2nmolNO同时生成nmolO2 |
| D.混合气体的颜色变浅 |
在一密闭容器中,用等物质的量的A和B发生如下反应:
A(g)+2B(g)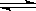 2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为:( )
2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为:( )
| A.40% | B.50% | C.60% | D.70% |
可逆反应:3 A(气)  3 B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量变小,则下列判断正确的是
3 B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量变小,则下列判断正确的是
| A.B和C可能都是固体 | B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 | D.B和C可能都是液体 |
一定温度下反应:A2(g)+3 B2(g) 2 AB3(g)(每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
2 AB3(g)(每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
| A.Q2 =" 2" Q1 | B.2Q1 < Q2 |
| C.Q1 < Q2 < 92.4 kJ | D.Q1 = Q2 < 92.4 kJ |
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应2SO2(g)+O2(g) 2SO3(g) ∆H=-196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) ∆H=-196kJ·moL−1,一段时间后达平衡,反应过程中测定的部分数据见下表:
| 反应时间/min |
n(SO2)/mol |
n(O2)/mol |
| 0 |
2 |
1 |
| 5 |
1.2 |
|
| 10 |
|
0.4 |
| 15 |
0.8 |
|
下列说法不正确的是
A.反应在前5min的平均速率为v (SO2)=0.08mol·L−1 ·min−1
B.保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)> v (逆)
C.该温度,反应的平衡常数为11.25L·mol-1
D.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知
 kJ·mol
kJ·mol )
)
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1mol N2、3mol H2 |
2mol NH3 |
4mol NH3 |
NH3的浓度(mol·L ) ) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出akJ |
吸收bkJ |
吸收ckJ |
| 体系压强(Pa) |
p1 |
p2 |
p3 |
| 反应物转化率 |
 |
 |
 |
下列说法正确的是
A. B.
B. C.
C. D.
D.
在容积固定的容器中发生反应:A(g)+2B(g)  C (g) ΔH<0,各物质浓度如表所示:
C (g) ΔH<0,各物质浓度如表所示:
| 浓度 时间 |
c(A)/mol·L-1 |
c(B)/mol·L-1 |
c(C)/mol·L-1 |
| 0 |
0.8 |
1.6 |
0 |
| 2 min |
0.6 |
x |
0.2 |
| 4 min |
0.3 |
0.6 |
0.5 |
| 6 min |
0.3 |
0.6 |
0.5 |
下列说法错误的是
A.2~4 min内用B表示的平均反应速率为0.3 mol·L-1·min-1
B.反应在第2 min时改变了条件,可能是加入了催化剂
C.反应在第2 min时改变了条件,可能是增加了B的浓度
D.若加入催化剂,平衡时气体混合物的总物质的量保持不变
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g) COS(g)+H2(g) K=0.1。反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g) K=0.1。反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
| A.建立平衡过程中,CO减少的浓度大于H2S减少的浓度 |
| B.通入CO后重新达平衡,正、逆反应速率均增大 |
| C.反应前H2S物质的量为7mol |
| D.CO的平衡转化率为80% |
反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,正确的是
C(g) +D(g)过程中的能量变化如图所示,正确的是
| A.该反应是吸热反应 |
| B.当反应达到平衡时,升高温度,A的转化率增大 |
| C.反应体系中加入催化剂对反应热没有影响 |
| D.在反应体系中加催化剂,反应速率增大,E1、E2均减小 |
在相同温度相同体积的甲、乙两容器中发生反应2SO2(g)+O2(g)  2SO3 (g),甲容器中充入1molSO2和1molO2,乙容器充入2molSO2和2molO2。下列叙述错误的是
2SO3 (g),甲容器中充入1molSO2和1molO2,乙容器充入2molSO2和2molO2。下列叙述错误的是
| A.化学反应速率:乙>甲 | B.平衡后O2的浓度:乙>甲 |
| C.平衡后SO2的转化率:乙>甲 | D.平衡后混合气体的密度:乙>2甲 |
在密闭容器中发生反应:aX(g)+bY(g) cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的物质的量浓度为原平衡的1.8倍。下列叙述中不正确的是
cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的物质的量浓度为原平衡的1.8倍。下列叙述中不正确的是
| A.平衡向逆反应方向移动 | B.a + b < c + d |
| C.Y的体积分数减小 | D.X的转化率下降 |
下列事实中,不能用勒夏特列原理解释的是
| A.冰镇的啤酒打开后泛起泡沫 |
B.对N2+3H2 2NH3的反应,使用铁触媒可加快合成氨反应的速率 2NH3的反应,使用铁触媒可加快合成氨反应的速率 |
C.工业制取金属钾Na(l)+KCl(l)  NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 |
D.氯水中存在如下平衡:Cl2+H2O HCl+HClO,当加入NaOH溶液后颜色变浅 HCl+HClO,当加入NaOH溶液后颜色变浅 |
制取水煤气的反应为C(s)+H2O(g) 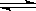 CO(g)+H2(g) △H > 0,欲提高反应的速率和C(s)的转化率,可采用的措施为
CO(g)+H2(g) △H > 0,欲提高反应的速率和C(s)的转化率,可采用的措施为
| A.降温 | B.增大水蒸气的浓度 | C.增大C(s)的量 | D.增大压强 |
1000K时,反应C(s)+2H2(g)  CH4(g)的 K=8.28×107,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述平衡
CH4(g)的 K=8.28×107,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述平衡
| A.向正反应方向移动 | B.向逆反应方向移动 |
| C.达到平衡 | D.无法判断移动方向 |
可逆反应A(g)+3B(g) 2C(g);ΔH=-Q kJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1 kJ在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
2C(g);ΔH=-Q kJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1 kJ在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75%
B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25 molA、0.75molB 、1.5molC,平衡向正反应方向移动
D.乙中的热化学反应方程式为2C(g) aA(g)+3B(g);ΔH=+Q2kJ·mol-1
aA(g)+3B(g);ΔH=+Q2kJ·mol-1