已知两瓶气体,分别是HCl和Cl2。可以区别它们的方法或试剂是
① 观察颜色 ②打开瓶盖看有无白雾 ③湿润的淀粉试纸
④湿润的红色石蕊试纸 ⑤湿润的蓝色石蕊试纸 ⑥硝酸银溶液
| A.①②③④ | B.①②⑤⑥ | C.①②④⑤ | D.①②④⑥ |
下列反应中不属于化合、分解、置换、复分解等四种基本反应类型的是
| A.CuSO4 + H2S =" CuS↓" + H2SO4 | B.2FeCl3 + Cu = 2FeCl2 + CuCl2 |
| C.Cu2(OH)2CO3=" 2CuO" + CO2↑ + H2O | D.4Fe(OH)2 + O2+ 2H2O = 4Fe(OH)3 |
下列关于化学观或化学研究方法的叙述中,正确的是 ( )
| A.随着化学的发展,化学实验方法并不是化学研究的唯一手段 |
| B.研究质子和中子的结构是化学科学研究的一项新任务 |
| C.根据盖斯定律,燃烧一定量的煤和燃烧同量的煤干馏后的焦炭产生的热量一样多 |
| D.在通风橱进行有毒气体的实验是一种符合“绿色化学”思想的防污染手段 |
假设某化学反应的反应过程如下图表示:( )
观察分析,符合图中变化的化学反应为
A.A2+3B2 2AB3 2AB3 |
B.2AB2+B2 2AB3 2AB3 |
| C.2A2B+5B2 =4AB3 | D.2AB2+B2 = 2AB3 |
考查以下涉及H2O2的反应(未配平):
①Na2O2+HCl H2O2+NaCl
H2O2+NaCl
②Ag2O+H2O2 Ag+O2↑+H2O
Ag+O2↑+H2O
③H2O2 H2O+O2↑
H2O+O2↑
④H2O2+Cr2(SO4)3+KOH K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
判断下列说法正确的是 ( )
| A.都是氧化还原反应 | B.反应④中还原性:H2O > Cr2(SO4)3 |
| C.发生还原反应的元素相同 | D.H2O2既有氧化性,又有还原性 |
下列化学用语表达不正确的是
A.Na+的结构示意图:  |
B.水分子的电子式: |
| C.二氧化碳的结构式:O=C=O | D.碳酸氢钠的电离方程式:NaHCO3= Na+ + HCO3ˉ |
已知阿伏伽德罗常数为NA,下列说法中正确的是( )
| A.常温常压下,当活泼金属转移2NA电子时,可从盐酸中置换产生22.4L H2 |
| B.100g98% 的浓硫酸中含有氧原子个数为4NA |
| C.CO与N2具有相同的电子总数,那么1molN2和22.4L的 CO气体所含有的电子总数为28NA |
| D.室温下,21.0g乙烯和丁烯(C4H8)的混合气体中含有的碳原子数目是1.5NA |
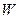 g某元素(无同位素)所含原子数目为
g某元素(无同位素)所含原子数目为 ,该元素原子的摩尔质量为
,该元素原子的摩尔质量为 g/mol ,则氯元素的一种同位素
g/mol ,则氯元素的一种同位素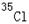 的一个原子的质量是( )(注:该Cl原子的相对原子质量≈35)
的一个原子的质量是( )(注:该Cl原子的相对原子质量≈35)
A. g g |
B.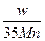 g g |
C.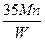 g g |
D.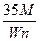 g g |
判断下列说法正确的是( )
| A.1molFeCl3跟水完全反应转化为氢氧化铁胶体,其中胶体粒子的物质的量为1mol |
| B.一定温度下,1L0.50mol/L NH4Cl 溶液与2L0.25mol/LNH4Cl溶液含有的NH4+的物质的量不同 |
| C.配制480mL 0.5mol/L 的CuSO4溶液,需要称取60.0g的CuSO4·5H2O晶体 |
| D.10mL质量分数为98% 的H2SO4溶液,用水稀释至100mL溶质质量分数变为9.8% |
(注:硫酸溶液的密度随浓度的增大而增大)
已知阿伏伽德罗常数为NA,下列说法中正确的是( )
| A.常温常压下,当活泼金属转移2NA电子时,可从盐酸中置换产生22.4L H2 |
| B.100g98% 的浓硫酸中含有氧原子个数为4NA |
| C.CO与N2具有相同的电子总数,那么1molN2和22.4L的 CO气体所含有的电子总数为28NA |
| D.室温下,21.0g乙烯和丁烯(C4H8)的混合气体中含有的碳原子数目是1.5NA |
现有一种溶液,其中可能含有Mg2+、Al3+、Fe2+、Cu2+、NH4+。当加入一种淡黄色固体并加热溶解时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示。试回答下列问题:
(1)最终的白色沉淀的成分是(填化学式) ,你的理由是 
(2)试确定该溶液中可能含有以上离子中的哪些离子并计算其相应的物质的量,完成下表(可以不填满)
| 可能含有的离子 (填离子符号) |
|
|
|
|
|
| 相应的物质的量 |
|
|
|
|
|
(4)图中a点的值为
(5)图中b点的气体组成成分是(填化学式) ,其物质的量之比是
下列有关化学用语表示正确的是
A.N2的电子式: |
B.S2-的结构示意图: |
| C.质子数为53,中子数为78的碘原子:53131I |
| D.乙烯的结构简式:CH2CH2 |
下列说法正确的是( )
| A.4.2 g丙烯中所含的共价键数目为0.6×6.02×1023 |
| B.含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023 |
| C.相同条件下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 |
| D.相同物质的量的OH-和CH3+含有相同数目的电子 |
下列选项错误的是
| A.在NH4C1晶体中含有离子键和共价键 |
| B.设想把“H2+Cl2 |
| C.某反应△H>0,△S>0,该反应是个非自发反应 |
| D.25℃时,NaNO2溶液的pH=8,c(Na+)-c(NO2-)=9.9×10-7mol·L-1 |