常温下,将amol.LNH3·H2O与b mol/LHCl (0<a<0.2,0<b<0.2)等体积混合,下列有关推论不正确的是 ( )
| A.若混合后溶液pH=7,则c(NH4+)=c(Cl-) |
B.若a="2b," 则c(Cl-)>c(NH4+)>c(NH3·H 2O)>c(OH-)>c(H+) 2O)>c(OH-)>c(H+) |
| C.若b=2a,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=b |
下列化学用语不正确的是
| A.漂粉精的主要成分:CaCl2 |
| B.乙烯的结构简式:CH2=CH2 |
C.Na+的结构示意图: |
D.原子核内有10个中子的氧原子: |
某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物 ②煤和石油都是可再生能源 ③不锈钢和目前流通的硬币都是合金④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑤蛋白质溶液、淀粉溶液和雾都是胶体。上述说法正确的是
| A.①③⑤ | B.①②④ | C.②③④ | D.③④⑤ |
下列化学用语使用正确的是 ( )
A.质量数为37的氯原子: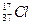 |
B.Ca2+的结构示意图为: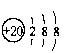 |
C.氢氧化钠的电子式: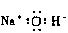 |
| D.乙烯的结构简式:CH2CH |
下列化学用语或命名正确的是 ( )
A.Cl-的结构示意图: |
B.NH4Cl的电子式: |
| C.丙烯的实验式(最简式):CH2 | D. 的名称:2-乙基丙烷 的名称:2-乙基丙烷 |
下列对化学知识的总结,你认为合理的组合是 ( )
①能与酸反应的氧化物,一定是碱性氧化物
②原子晶体、离子晶体、金属晶体、分子晶体 中都一定存在化学键
中都一定存在化学键
③原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
④在熔化状态或水溶液中能导电的物质称为电解质
⑤NF3的沸点比NH3的沸点低是因为N-F键比N-H键的键能大
⑥过氧化氢和液氮的分子中都有非极性共价键
| A.只有③④ | B.只有③⑥ |
| C.只有⑤⑥ | D.只有①②⑥ |
用惰性电极电解2L硝酸银溶液,当在电路中通过0.1mol电子后,调换正负极,电路中又通过了0.2mol电子,此时溶液pH值为(假设溶液体积不变)是
| A.2 | B.3 | C.1 | D.无法确定 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是: ( )
| A.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B.标准状况下,22.4L己烷中共价键数目为19NA |
| C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32- |
在三个密闭容器中分别充入CO、CH4、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是 ( )
| A.p(CO)>p(CH4)>p(O2) | B.p(O2)>p(CO)>p(CH4) |
| C.p(CH4)>p(O2)>p(CO) | D.p(CH4)>p(CO)>p(O2) |
含有11.2 g KOH的稀溶液与1 L 0.1 mol· L-1的H2SO4溶液反应放出11.46 kJ的热量,表示该反应的中和热的热化学方程式为( )
A.KOH(aq)+1/2H2SO4(aq) 1/2K2SO4(aq)+H2O(l);ΔH=-11.46 kJ· mol-1 1/2K2SO4(aq)+H2O(l);ΔH=-11.46 kJ· mol-1 |
B.2 KOH(aq)+H2SO4(aq) K2SO4(aq)+2H2O(l);ΔH=-114.6 kJ· mol-1 K2SO4(aq)+2H2O(l);ΔH=-114.6 kJ· mol-1 |
C.2KOH(aq)+H2SO4(aq) K2 K2 SO4(aq)+2H2O(l);ΔH=+114.6 kJ· mol-1 SO4(aq)+2H2O(l);ΔH=+114.6 kJ· mol-1 |
D.KOH(aq)+1/2H2SO4(aq) 1/2K2SO4(aq)+H2O(l);ΔH=- 1/2K2SO4(aq)+H2O(l);ΔH=- 57.3 kJ· mol-1 57.3 kJ· mol-1 |
将7g炭粉与14g氧气在一定条件下完全反生成21g氧化物,则生成物中CO与CO2的物质的量之比为
| A.1:1 | B.2:1 | C.2:3 | D.3:1 |
在化合物A2B和BC2中,B的质量分数分别约为20%和30%,则在化合物A2BC3中B的质量分数最接近
| A.5% | B.10% | C.15% | D.20% |
下列说法不正确的是
| A.化学反应过程中的能量变化除了热能外,也可以是光能、电能等 |
| B.吸热反应一定不能在常温下进行 |
| C.需要加热才能进行的反应不一定是吸热反应 |
| D.反应物总能量高于生成物总能量的反应是放热反应 |