在t℃时,将 a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为 b moL。下列叙述中正确的是( )
A.溶质的质量分数为ω= |
B.溶质的物质的量浓度 |
C.溶液中c(OH-)= |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
100mL 0.3mol·L-1Na2SO4溶液和50mL 0.2mol·L-1Al2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度为( )
| A.0.20mol·L-1 | B.0.25mol·L-1 | C.0.40mol·L-1 | D.0.50mol·L-1 |
用NaOH固体配制1.0 mol·L-1的NaOH溶液220mL,下列说法正确的是( )
| A.首先称取NaOH固体8.8g |
| B.定容时仰视刻度线会使所配制的溶液浓度偏高 |
| C.定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线 |
| D.容量瓶中原有少量蒸馏水没有影响。 |
相同质量的CuO和MgO粉末分别溶于相同体积的硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1。则a与b的关系为 ( )
| A.a="b" | B.a="2b" | C.2a="b" | D.a=5b |
质量分数为a的某物质的溶液mg与质量分数为b的该物质的溶液ng混合后,蒸发掉pg水,得到的溶液每毫升质量为qg,物质的量浓度为c。则溶质的相对分子质量为( )
A.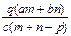 |
B.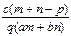 |
C.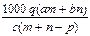 |
D.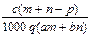 |
下列说法正确的是( )
| A.pH=2和pH=1的硝酸中c(H+)之比为1︰10 |
B.Na2CO3溶液c(Na+)与c(CO )之比为2︰1 )之比为2︰1 |
| C.0.2 mol·L-1与0.1 mol·L-1醋酸中c(H+)之比为2︰1 |
| D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3︰1 |
用1000g溶剂中所含溶质的物质的量来表示的溶液浓度叫做质量物质的量浓度,其单位是mol/kg。5mol/kg的硫酸的密度是1.2894g/cm3,则其物质的量浓度是( )
| A.3.56mol/L | B.5.23mol/L | C.4.33mol/L | D.5.00mol/L |
等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1︰2︰3,则三种硫酸盐溶液的物质的量浓度之比为( )
| A.1︰2︰3 | B.1︰6︰9 | C.1︰3︰3 | D.1︰3︰6 |
某氯化镁溶液的密度为1.18g•cm-1,其中镁离子的质量分数为5.1%。300mL该溶液中Cl-离子的物质的量约等于( )
| A.0.37mol | B.0.63mol | C.0.74mol | D.1.5mol |
用食用白醋(醋酸浓度约1 )进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入豆浆中有沉淀产生 |
| C. | 蛋壳浸泡在白醋中有气体放出 | D. |
|