乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答: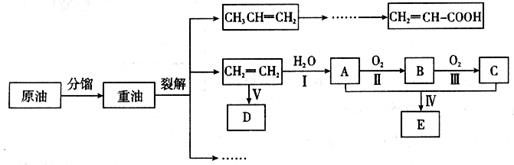
已知:
(1)写出A的电子式 。
(2)反应II的化学方程式是__________。
(3)D为高分子化合物,可以用来制造多种包装材料,其结构简式是__________。
(4)E是有香味的物质,在实验室用下图装置制取。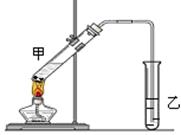
①反应IV的化学方程式是__________,该反应类型为______。
②该装置图中有一个明显的错误是 。
(5)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
| 实验编号 |
试管甲中试剂 |
试管乙中试剂 |
有机层的厚度/cm |
| A |
2 mL乙醇、1 mL乙酸、 1mL18mol·L-1浓硫酸 |
饱和Na2CO3溶液 |
3.0 |
| B |
2 mL乙醇、1 mL乙酸 |
0.1 |
|
| C |
2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 |
0.6 |
|
| D |
2 mL乙醇、1 mL乙酸、盐酸 |
0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是3mL和_____mol·L-1。
②分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(共15分)不饱和酯类化合物在药物、涂料等领域应用广泛。
(1)下列关于化合物I的说法,正确的是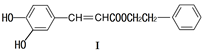
| A.可能发生酯化反应和银镜反应 |
| B.1mol化合物I最多与2molNaOH反应 |
| C.与FeCl3溶液能显紫色 |
| D.能与溴发生取代和加成反应 |
(2)下面反应是一种由烯烃直接制备不饱和酯的新方法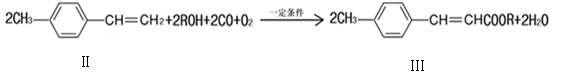
①化合物II的分子式为 。
②1mol化合物II能与 molH2恰好反应生成饱和烃类化合物。
③化合物Ⅲ与足量的NaOH溶液共热的化学方程式为 ;反应类型:
(3)3﹣对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下: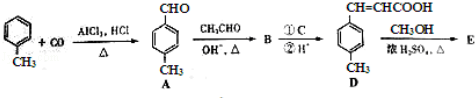
已知:HCHO+CH3CHO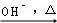 CH2=CHCHO+H2O
CH2=CHCHO+H2O
①A中官能团的名称为 。D中含氧官能团的名称为 。
②E的结构简式为 。
③试剂C可选用下列中的
a、溴水 b、银氨溶液
c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液
④B在一定条件下可以生成高聚物F,该反应的化学方程式为_________ 。