下列热化学方程式书写正确的是
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H="—1367.0" kJ/mol |
| B.HCl (aq)+NaOH(ag)=NaCl(ag)+H2O(1)△H=+57.3kJ/mol |
| C.S(s)+O2(g)=SO2(g)△H= —296.8kJ |
| D.2NO2=O2+2NO△H=+116.2kJ/mol |
下列图像分别表示有关反应的反应过程与能量变化的关系

据此判断下列说法中正确的是
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.S(g) ===" S(s)" ΔH > 0 |
| D.H2(g)+I2(g) ===" 2HI(g)" ΔH > 0 |
设计实验证明:某种盐的水解吸热。有四位同学分别作出如下回答,错误的是
| A.甲同学:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解吸热 |
B.乙同学:用加热的 方法可除去KNO3溶液中混有的Fe3+,说明含Fe3+的盐水解吸热 方法可除去KNO3溶液中混有的Fe3+,说明含Fe3+的盐水解吸热 |
| C.丙同学:通过实验发现同浓度的热的纯碱液比冷的纯碱液去油污效果好,说明碳酸钠水解吸热 |
| D.丁同学:在纯碱液中滴入酚酞试液,加热(不考虑水蒸发)后若红色加深,说明碳酸钠水解吸热 |
下列反应中反应物总能量高于生成物总能量的是 ( )
| A.二氧化碳与碳生成一氧化碳 | B.碳与水蒸气生成一氧化碳和氢气 |
C.碳酸钙受热分解 |
D.盐酸与氢氧化钠反应 |
Ⅰ、恒温、恒压下,在一个可变容积的容器中发生如下反应: N2(g)+3H2(g) 2NH3(g); △H<0
2NH3(g); △H<0
(1)工业生产中,该反应通常在高压下进行反应,做出此选择的理由是:
① ;
② 。
(2)开始时放入1mol N2和3mol H2,到达平衡后,生成amol NH3,若开始时放入χmol N2、3mol H2和y mol NH3,到达平衡后,NH3的物质的量为 3amol,则x= mol,y= mol。
Ⅱ、若该容器恒压、绝热(与外界不发生热交换),在一个与(2)反应前起始条件完全相同的容器中发生上述反应
(3)若开始时放入1mol N2和3mol H2,到达平衡后,生成b mol NH3,将b与(2)小题中的a进行比较 (选填一个编号)
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
Ⅲ、某研究性学习小组为探究利用电化学原理合成氨,设计如图所示的装置,
(4)电极B为 极
(5)电极A发生的电极反应式为
(6)该电池工作一段时间后,电解质溶液pH
(填增大、减小或不变)
下列反应属于吸热反应的是 ( )
A.C6H12O6(葡萄糖aq)+6O2 6CO2+6H2O 6CO2+6H2O |
| B.CH3COOH+KOH=CH3COOK+H2O |
| C.A+B=C+D;ΔH <0 |
| D.反应物的键能大于生成物的键能 |
下列说法中正确的是( )
| A.任何化学反应都伴随着能量的变化 |
| B.1 mol H2SO4和1 mol Ba(OH)2完全反应所放出的热量称为中和热 |
| C.在101 kPa时,1 mol碳燃烧放出的热量就是碳的燃烧热 |
| D.热化学方程式未注明温度和压强时,ΔH表示标准状况下的数据 |
碳和碳的化合物在人类生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l);△H1= —1214kJ/mol
②2CO(g)+O2(g)=2CO2(g);△H2= —566kJ/mol
则反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H= 。
(2)①将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其正极电极反应式是: 。
②某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)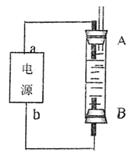
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-→H2↑
③若将 所得Fe(OH)2沉淀暴露在空气中,反应的化学方程式为 。
所得Fe(OH)2沉淀暴露在空气中,反应的化学方程式为 。
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
|
| H2O |
CO |
CO2 |
|||
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
a |
b |
c |
1 |
①实验1中,以v(H2)表示的平均反应速率为 。
②该反应的正反应为 (填“吸”或“放”)热反应。
(4)将2.4g碳(碳的相对原子质量为12)在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,溶液中的溶质的化学式是 ;溶液中所含离子的物质的量浓度由大到小的顺序为: 。
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池.
①当电解质溶液为稀硫酸时:
Cu电极是_____(填“正”或“负”)极,其电极反应为____,该反应是____(填“氧化”或“还原”)反应;
②当电解质溶液为浓硝酸时:
Cu电极是_____极,其电极反应为__________,该反应是_____反应.
(2)电解是将 能转化为 能。请写出电解硫酸铜溶液的总化学方程式____________
(3)燃烧氢气时耗氧量小,发热量大.已知4克H2燃烧生成液态水时放热为571.6kJ,试写出表示H2燃烧热的热化学方程式为: .
(4)下图是一碳酸盐燃料电池(MCFC),以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出B极发生的电极反应式 。
0.3 mol硼烷(B2H6)在氧气中完全燃烧生成固体B2O3和液态水,放出649.5 kJ热量。下列判断正确的是
| A.该反应是非氧化还原反应 |
| B.在理论上可以利用该反应的原理做成燃料电池 |
C.该反应的热化学方程式为:B2H6+3O2="==" B2O3(s)+3H2O(l); H="-2165" kJ/mol H="-2165" kJ/mol |
| D.每生成18g水,该反应转移2mol电子 |
金刚石与石墨是碳的两种同素异形体,在100 kPa时,1mol石墨转化为金刚石要吸收1.895 kJ的热量,下列说法正确的是
| A.金刚石比石墨稳定 | B.1mol石墨比1mol金刚石的总能量低 |
| C.1mol石墨比1mol金刚石的总能量高 | D.石墨比金刚石稳定 |
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出肼和过氧化氢的电子式:肼___________________,过氧化氢______________ 。
(2)写出该反应热化学方程式:________________________________________________。
(3)已知H2O(1)==H2O(g) △H=+44kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_____________________ kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体外,还有一个很突出的优点是:_____________________________________________________________________。
2008年初,中国南方的大雪引发了巨大灾难。下列说法不正确的是
| A.雪是由水蒸气凝华而成的,该过程有能量放出 |
| B.雪融化为水后能量增加 |
| C.雪融化为水时要吸收能量,导致环境温度升高 |
| D.在雪上撒大量的以NaCl、MgCl2等为主要成分的融雪剂 |