下图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质,而I是红棕色的气态氧化物。固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D。各物质间的转化关系如下图所示:
请回答下列问题: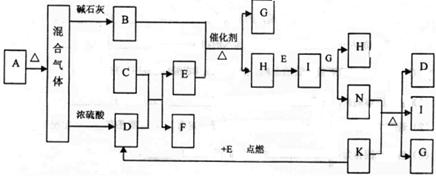
(1)写出实验室检验A物质中含有的阳离子的方法 。
(2)B与E反应得到1mol H,则此时转移电子的物质的量为 mol。
(3)写出实验室制取B的化学方程式 。
(4)写出N的稀溶液与过量的铁粉反应的离子方程式 。
(5)若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8:5,则用物质的量的关系表示此固体A的组成为 。
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第 周期、第 族;
(2)写出反应①的化学方程式 ;
(3)写出反应④的离子方程式 ;
(4)写出反应③的电极方程式:
阳极: 阴极:
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是 。(填序号)
下图中,B、D、E、F、G是氧化物,F和K都是氢化物,C、H是日常生活中最常见的金属单质,J是气态非金属单质,其水溶液与D均具有漂白性。O是白色沉淀,在空气中很容易转化为N,且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品,其工业制备过程包括反应⑤和⑥(图中部分反应物和生成物没有列出)。请按要求回答:
(1)写出L的化学式: 。
(2)写出:反应③的离子方程式 ;
反应④的化学方程式 ;
反应④的现象是 。
(3)反应②在工业生产上的用途是 。
(4)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1:1:1:14,则反应①的化学方程式为 。
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,F为红棕色气体,H为黑色固体,B为白色沉淀。D、H都是常见的非金属单质。
请回答下列问题:
(1)J的电子式为____________________。
(2)F的化学式为____________________。
(3)写出K加热生成L化学方程式:_____________________________________。
(4)写出B与过量NaOH溶液反应生成C的离子方程式:_______________________。
(12分)已知A为蓝色溶液,B、C、I、K为单质,其余均为化合物,其中B、L、I、K 常温下为气体,且I为有色气体。G为黑色固体,F的焰色反应透过蓝色钻玻璃片显紫色,各物质转化关系如图。
回答下列问题:
(1)P的电子式是_________________;
(2)C元素原子价电子排布式为: 。
(3)已知B、H和C2H5OH能够组成燃料电池,写出该燃料电池的负极反应式:
_______________________________________________________________;
(4)A的水溶液呈___________(填“酸性”“碱性”“中性”),用离子方程式和必要的文字说明原因______________________________________________________________
(5)用惰性电极电解400.00 mL A溶液,一段时间内测得溶液pH=1,则需要向溶液中加入___________,其质量为______g,才能使溶液恢复到电解前的状态(不考虑溶液体积变化)。
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体, C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
(1)写出下列物质的化学式:
A: D: R: 。
(2)按要求写下列反应方程式:
H并在潮湿空气中变成M的过程中的化学方程式: ;
B和R反应生成N的离子方程式: ;
D与盐酸反应的离子方程式: 。
(3)检验气体C的方法: 。
(14分)A、J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极;F常温下是气体,各物质有如图所示的转化关系(部分产物及条件略去)。
请回答以下问题:
(1)写出原电池的负极反应方程式
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为 (写出计算式);相同条件下,等浓度的c溶液与CH3COONa溶液中,C的阴离子与CH3COO一浓度的大小关系:前者 后者(用“>”“<”或“=”表示)。
(3)写出②的化学方程式
(4)含A元素的某盐x常作净水剂,x做焰色反应时,透过
蓝色的钴玻璃观察火焰呈紫色。
①x的水溶液与NaHCO3溶液混合,反应的离子方程式为
②500mL X的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图,x晶体的俗名为 ;其溶液的物质的量浓度为 mol/L。
图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
回答下列问题:
(1)组成单质Z的元素在周期表中的位置是 ; R的化学式是 ;
(2)E、Z的晶体类型均属于 晶体。E、Z结构中最小的环上原子个数之比为
。B为一元强碱,焰色反应为紫色,则B的电子式为 。
(3)写出下列反应的化学方程式:
①单质Z与 NaOH的反应:
②工业上由E制取粗Z:
(4)已知A与1 mol Al反应转化为X时(所有物质均为固体),放出a kJ 热量,写出该反应的热化学方程式: 。
(5)向A与X的混合物中加入100 mL 1mol / L盐酸恰好使混合物完全溶解,放出标准状况下的气体224 mL,在溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到单质的质量为 。
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈、烧杯和玻璃棒,还要补充的玻璃仪器是 。
(2)如何用实验证明沉淀D已洗涤干净 。
(3)由滤液A制得AlCl3溶液有途径I和Ⅱ两条,你认为合理的是途径 (填写“I”或“Ⅱ”),理由是 ;请写出途径Ⅱ得到沉淀D的离子方程式 。
(4)从滤液E中得到绿矾晶体的实验操作是蒸发浓缩、 、过滤。
(5)有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,但前者的方案更合理,理由是 。
| A.后者消耗的酸和碱更多 | B.后者难以实现物质分离 |
| C.前者制得的产物更纯净 | D.前者操作步骤更少,方案简单 |
已知A、B、C、D、E、F、G、H 可以发生如下图所示的转化,反应中部分生成物已略去。其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。
请填空:
(1)反应①的化学方程式是 。
(2)反应④的离子方程式是 。
(3)写出反应③的化学方程式并标明电子转移方向及数目 。
(4)设计实验证明反应③的气体产物中既有B,又有C,可将气体依次通过:溶液Ⅰ、酸性高锰酸钾溶液、溶液Ⅰ、溶液Ⅱ,则溶液Ⅰ和溶液Ⅱ分别为(填试剂名称): 、 ,实验中两次使用溶液Ⅰ的作用分别是 , 。
(5)在工业生产上规定:空气中C的最大允许排放浓度不得超过0.02mg/L。
某同学拟用下列简易装置测定空气中C的含量:准确移取50mL 1×10-4mol/L的标准碘水溶液,注入下图所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色。在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n)。反应中碘发生的变化为I2→HI。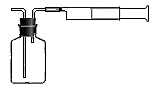
①写出C与碘水反应的化学方程式 ;
②若测得抽气次数为100,则空气中C的含量为 mg/L;
③乙同学抽气的次数至少为 次,方可说明该地空气中C的含量符合排放标准。
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75% ,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为无色液体。反应生成的水均已略去。它们有如下图所示的关系。
(1)写出化学式:A B J 。
(2)反应③中每生成1molF,转移电子的数目为: 。
(3)反应④的化学方程式为: 。
(4)离子方程式分别为:反应② ;
⑤ 。
(5)反应①中,每1.00gC与足量的F作用,恢复到25oC放出55.6kJ热量,写出反应①的热化学方程式 。
已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):
请填写下列空白:
(1)金属A为 ;操作a是将D溶液在HCl气流中蒸干,原因是
(2)反应②的化学方程为: ;
反应⑤的化学方程: 。
(3)原电池反应①中,正极反应式为: 。
下列框图中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H是呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。
(1)写出H的化学式: 、C的电子式: 。
(2)写出D与I溶液发生反应的离子方程式: 。
(3)写出L→M的化学方程式: 。
(4)检验J中的阳离子时,不宜选用下列试剂中的 (填选项字母)。
A.Fe粉 B.NaOH溶液 C.KSCN溶液
某些化学反应可用下式表示A+B→→C+D+H2O。请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
(3)若A、C均含有铝元素。①当B是盐酸时,C是 ;
②当B是NaOH时,C是 。
(14)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如图所示:
请回答下列问题:
(1)元素A在元素周期表中的位置为 周期 族。
(2)写出K的电子式 。
(3)写出H和D反应的化学方程式 。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 。
(5)写出A与G反应的化学方程式 。
(6)K与E反应时产生的现象有 ;该反应的化学方程式为 ___________________。
(7)已知F的燃烧热为akJ/mol,L的燃烧热为bkJ/mol,试写出F生成L的热化学方程式_________________