(6分)有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:
⑴取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
⑵继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
⑶取少量(2)中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶。
根据上述实验现象判断:该白色固体中一定含有 ,一定不含有 ,可能含有 。
下图中A~J均代表无机物或其水溶液,其中A是一种红棕色粉末,B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。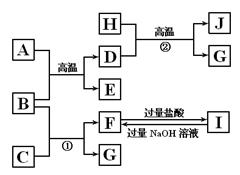
根据图示回答问题:
(1)写出下列物质的化学式:A ,E ,I ;
(2)反应①的化学方程式是 ;
反应②的化学方程式是 ;
(3)J与盐酸反应的离子方程式是 ;
反应后的溶液与D反应的化学方程式是 。
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应②是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F、P 和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为常见的致冷剂,化合物M由两种元素组成,分子内共有58个电子。

(1)化合物A中含有的两种元素是 (写元素符号)M的化学式_______
(2)如何检验化合物N中的阳离子
(3)写出K与H反应的离子方程式:
C与D反应的化学方程式:
(4)等物质的量F和H的混合气体通入品红溶液中的现象为 ,原因是(用离子反应方程式表示)
(5)实验中可用NaOH溶液来吸收多余的H,请写出此离子反应方程式
(2分)
EDTA是乙二胺四乙酸的英文名称的缩写,市售试剂是其二水合二钠盐。
⑴画出EDTA二钠盐水溶液中浓度最高的阴离子的结构简式。
⑵ Ca(EDTA)2-溶液可用于静脉点滴以排除体内的铅。写出这个排铅反应的化学方程式(用Pb2+ 表示铅)。
⑶能否用EDTA二钠盐溶液代替Ca(EDTA) 2-溶液排铅?为什么?氨和三氧化硫反应得到一种晶体,熔点205oC,不含结晶水。晶体中的分子有一个三重旋转轴,有极性。画出这种分子的结构式,标出正负极。
Na2[Fe(CN)5(NO)]的磁矩为零,给出铁原子的氧化态。Na2[Fe(CN)5(NO)]是鉴定S2-的试剂,二者反应得到紫色溶液,写出鉴定反应的离子方程式。
CaSO4 • 2H2O微溶于水,但在HNO3 ( 1 mol L1)、HClO4 ( 1 mol L-1)中可溶。写出能够解释CaSO4在酸中溶解的反应方程式。
取质量相等的2份PbSO4 (难溶物)粉末,分别加入HNO3 ( 3 mol L-1) 和HClO4 ( 3 mol L-1),充分混合,PbSO4在HNO3 能全溶,而在HClO4中不能全溶。简要解释PbSO4在HNO3中溶解的原因。
X和Y在周期表中相邻。CaCO3与X的单质高温反应,生成化合物B和一种气态氧化物;B与Y的单质反应生成化合物C和X的单质;B水解生成D;C水解生成E,E水解生成尿素。确定B、C、D、E、X和Y。