氮化硅硬度大、熔点高、不溶于酸(氢氟酸除外),是一种重要的结构陶瓷材料。一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺主要流程如下:

(1)净化N2和H2时,铜屑的作用是:_________________;硅胶的作用是 。
(2)在氮化炉中3Si(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度: ;
(3)X可能是 (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)
(4)如何说明氮化硅产品已用水洗干净? 。
(5)用硅粉作硅源、叠氮化钠(NaN3)作氮源,直接燃烧生成氮化硅(发生置换反应),该反应的化学方程式为: 。
将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是
| A.反应速率:两者相同 |
| B.消耗HNO3的物质的量:前者多,后者少 |
| C.反应生成气体的颜色:前者浅,后者深 |
| D.反应中转移的电子总数:前者多,后者少 |
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
| A.1∶7 | B.1∶9 | C.1∶5 | D.2∶9 |
将Mg和Cu组成的混合物7.64 g投入足量的稀硝酸中使其完全反应,得到的唯一还原产物NO在标准状况下体积为2.24 L。将反应后的溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO-3的浓度为
| A.0.3 mol/L | B.0.4 mol/L | C.0.5 mol/L | D.0.6 mol/L |
将0.4mol体积比为1∶1甲和乙两种混合气体同时通入50mL1mol·L-1的丙溶液中,无沉淀产生的是
| 序号 |
甲 |
乙 |
丙 |
| A |
Cl2 |
SO2 |
Ba(NO3) 2 |
| B |
HCl |
CO2 |
石灰水 |
| C |
NH3 |
SO2 |
Ba(OH)2 |
| D |
NO2 |
SO2 |
BaCl2 |
粒子甲在溶液中的转化关系如下图所示,粒子甲不可能是
| A.NH4 + | B.Al(OH)3 | C.S | D.Al |
下列现象或事实不能用同一原理解释的是
| A.浓硝酸和氯水用棕色试剂瓶保存 |
| B.硫化钠和亚硫酸钠固体长期暴露在空气中变质 |
| C.常温下铁和铂都不溶于浓硝酸 |
| D.SO2和Na2SO3溶液都能使氯水褪色 |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体为
| A.2.24L | B.1.12L | C.0.672L | D.0.448L |
下图是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是

| |
甲 |
乙 |
丙 |
丁 |
| A |
FeCl3 |
FeCl2 |
Fe2O3 |
Fe(OH)3 |
| B |
Cu |
CuO |
CuSO4 |
CuCl2 |
| C |
NO |
HNO3 |
NO2 |
NH3 |
| D |
Si |
Na2SiO3 |
SiO2 |
SiF4 |
下列有关实验的叙述正确的是
| A.实验室中用生石灰与浓氨水混合的方法不能制得氨气 |
| B.中和滴定实验中,所用滴定管和锥形瓶均不能用待装液润洗 |
| C.在加热的情况下,烧瓶中的液体体积不要超过烧瓶容积的1/3 |
| D.将KI和FeCl3溶液混合后,加入CCl4振荡静置,下层液体变紫色,说明氧化性: Fe3+> I2 |
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,不一定能产生沉淀的是
| A.②④ | B.① | C.①③ | D.④ |
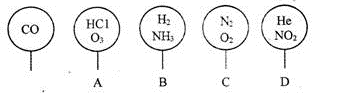
取五个相同的气球,同温同压下,分别充入CO和以下四种混合气体,吹出体积相等的状况,如图所示。A、B、C、D四个气球内,与CO所含原子数一定相等的是