常温下将NaOH溶液添加到己二酸( )溶液中,混合溶液的pH与离子浓度变化的关系如图所示.下列叙述错误的是( )
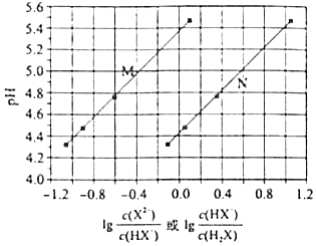
| A. | 的数量级为 |
| B. | 曲线N表示pH与 的变化关系 |
| C. | NaHX溶液中 |
| D. | 当混合溶液呈中性时, |
下列有关电解质溶液的说法正确的是( )
| A. | 向 溶液中加入少量水,溶液中 减小 |
| B. | 将 溶液从20℃升温至30℃,溶液中 增大 |
| C. | 向盐酸中加入氨水至中性,溶液中 >1 |
| D. | 向AgCl、AgBr的饱和溶液中加入少量 , 溶液中 不变 |
溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾
的
,
)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )

A.混合溶液的导电能力与离子浓度和种类有关
B. 与 的导电能力之和大于 的
C.b点的混合溶液
D.c点的混合溶液中,
298K时,在 氨水中滴入 的盐酸,溶液的 与所加盐酸的体积关系如图所示。已知 氨水的电离度为 ,下列有关叙述正确的是

| A. |
该滴定过程应该选择酚酞作为指示剂 |
| B. |
点对应的盐酸体积为 |
| C. |
点处的溶液中 |
| D. |
点处的溶液中 |
室温下,将两种浓度均为0.10mol•L﹣1的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCO3﹣Na2CO3混合溶液(pH=10.30):c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(OH﹣)
B.氨水﹣NH4Cl混合溶液(pH=9.25):c(NH4+)+c(H+)=c(NH3•H2O)+c(OH﹣)
C.CH3COOH﹣CH3COONa混合溶液(pH=4.76):c(Na+)>c(CH3COOH)>c(CH3COO﹣)>c(H+)
D.H2C2O4﹣NaHC2O4混合溶液(pH=1.68,H2C2O4为二元弱酸):c(H+)+c(H2C2O4)═c(Na+)+c(C2O42﹣)+c(OH﹣)