(1)室温下,有一pH=12的NaOH溶液100mL,欲使它的pH降为11。
①如果加入蒸馏水,就加入________mL
②如果加入pH=10的NaOH溶液,应加入_________mL
③如果加入0.008mol/LHCl溶液,应加入__________mL
(2)实验室在配制溶液时,一些物质存在水解的情况,如在配制Na2CO3溶液时,CO32-会水解,请书写水解离子方程式,在配制Al2(SO4)3溶液时,Al3+也存在水解,请书写水解离子方程式,为了防止Al2(SO4)3发生水解,可加入少量的。
(3)工业上用氧化铜制备氯化铜时,先将制的氧化铜(含有杂质FeO)用浓酸溶解得到的氯化铜(溶液中含有一定量的Fe2+)。
| 金属离子 |
pH值 |
|
| 开始沉淀 |
完全沉淀 |
|
| Fe2+ |
7.6 |
9.6 |
| Cu2+ |
4.4 |
6.4 |
| Fe3+ |
2.7 |
3.7 |
实际生产中先用次氯酸钠将Fe2+氧化成Fe3+,然后用试剂将溶液pH值调至 ~ ,即可除去铁杂质。
水解原理在工农业生产、日常生活中具有重要用途。下列关于物质的用途,与盐类水解有关的是
| A.次氯酸钠常用作消毒剂 | B.FeCl3用于印刷线路板 |
| C.热的纯碱溶液用于清洗油污 | D.氯化钠是氯碱工业的重要原料 |
下列离子方程式方程式中正确的是
A.NaHCO3溶液中HCO3-水解:HCO3-+ H2O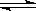 H2CO3+OH- H2CO3+OH- |
| B.AlCl3溶液中Al3+水解:Al3++3H2O = Al(OH)3↓+3H+ |
C.NaHS溶液中HS-水解:HS-+H2O 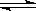 H3O++S2- H3O++S2- |
D.碳酸溶液中H2CO3的电离:H2CO3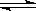 2H++ CO32- 2H++ CO32- |
化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
| 选项 |
现象或事实 |
解释或对应的方程式 |
| A |
用热的纯碱溶液洗去油污 |
CO32-+2H2O H2CO3+2OH- H2CO3+2OH-溶液呈碱性 |
| B |
酸雨样品在空气中放置pH减小 |
亚硫酸被氧化为硫酸2SO32-+O2=2SO42- |
| C |
“84”消毒液具有漂白性 |
2ClO-+CO2+H2O=2HClO+CO32- |
| D |
用加热法除去NaOH固体中混有的NH4Cl固体 |
NH4Cl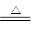 NH3↑+HCl↑ NH3↑+HCl↑ |
下列说法错误的是
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol•L﹣1的Na2CO3、NaHCO3混合溶液:2c(Na+)═3[c(CO32﹣)+c(HCO3﹣)]
③在0.1mol•L﹣1氨水中滴加0.lmol•L﹣1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH﹣)=l0﹣amol•L﹣1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32﹣)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH﹣)+c(H2S)+c(HS)
| A.①④ | B.②⑤ | C.①③ | D.②④ |
下列有关化学实验事实描述正确的是( )
A.Na2CO3溶液呈碱性的原因是:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| B.用NaAlO2溶液可以鉴别Na2CO3溶液和NaHCO3溶液 |
| C.有NH4+浓度相等的NH4Cl、CH3COONH4和NH4Al(SO4)2三种溶液,测得相同温度下溶质浓度最大的是NH4Al(SO4)2溶液 |
| D.AlCl3溶液和NaAlO2溶液加热蒸干所得主要成分都是Al(OH)3固体 |
在0.1mol/L的NaHCO3溶液中,下列关系式正确的是( )
| A.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-) |
| B.c(Na+)+ c(H+)=c(HCO3-)+c(OH-) |
| C.c(H2CO3)+c(H+)=c(OH-)+c(CO32-) |
| D.c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
向体积为Va的0.05 mol·L-1CH3COOH溶液中加入体积为Vb的0.05 mol·L-1KOH溶液,下列关系错误的是
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
实验室有下列试剂,其中必须用带橡胶塞的试剂瓶保存的是
①NaOH溶液;②水玻璃;③Na2S溶液;④Na2CO3溶液;
⑤NH4Cl溶液;⑥澄清石灰水;⑦浓HNO3;⑧浓H2SO4
| A.①⑥ | B.①②③④⑥ | C.①②③⑥⑦⑧ | D.⑤⑦⑧ |
常温下,0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液的叙述正确的是( )
| A.溶液中由水电离产生的H+浓度为1×10-7 mol/L |
| B.c(CH3COO-)+c(CH3COOH)-c(Na+)=0.05 mol/L |
| C.溶液中CH3COOH的电离程度小于CH3COONa的水解程度 |
| D.溶液中离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
下列过程或现象与盐类水解无关的是
| A.纯碱溶液去油污 | B.铁在潮湿的环境下生锈 |
| C.加热氯化铁溶液颜色变深 | D.浓硫化钠溶液有臭味 |
下列有关问题,与盐的水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
| A.②③④ | B.①②③④⑤ | C.①④⑤ | D.①②③ |
下列溶液中有关物质的量浓度关系正确的是( )
| A.碳酸氢钠溶液:c(Na+)+ c(H+)= c(CO32-)+ c(OH-)+ c(HCO3-) |
| B.物质的量浓度相等的CH3COOH和CH3COO Na 溶液等体积混合:c(CH3COOH)+ c(CH3COO-)="2" c(Na+) |
| C.硫酸铜溶液与过量浓氨水反应的离子方程式为:Cu2++ 2NH3•H2O= Cu(OH)2↓ +2 NH4+ |
| D.一定浓度的盐酸和氨水混合可能出现c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
电解质水溶液中可存在电离平衡,水解平衡,溶解平衡,依据所学回答下列问题。
(1)等物质的量浓度的下列四种溶液:①NH3·H2O ②(NH4)2SO3③KHSO3④K2SO3溶液中水的电离程度由大到小的排列顺序为________________(填序号)。
(2)体积相同、c(H+)相同的三种酸溶液①CH3COOH;②HCl;③H2SO4分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是(填序号) _____________。将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为_____________(填序号)。
(3)已知,H+ (aq) + OH-(aq) ="=" H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为____________。
(4)25℃时,NH3·H2O的电离常数为Kb=1.7×10-3。0.1mol·L-1NH4Cl溶液的pH=a,则c(NH4+)∶c(NH3·H2O)=_________(用含a的代数式表示)
(5)某化学研究性学习小组对电解质溶液作如下归纳总结(均在常温下),其中正确的有( )
①pH=1的强酸溶液,加水稀释后,溶液中各离子浓度一定都降低
②pH=2的盐酸与pH=13的NaOH溶液,按体积比9:1混合后的溶液pH为11
③pH相等的三种溶液:a.CH3COONa;b.NaHCO3;c.NaOH.其溶液物质的量浓度由小到大顺序为c、b、a
④NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO42﹣)
⑤亚磷酸(H3PO3)是二元弱酸,所以Na2HPO3稀溶液一定呈碱性
⑥甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙两溶液等体积混合,混合液pH可能等于7.
⑦某二元酸在水中的电离方程式是H2B═H++HB﹣;HB﹣ H++B2﹣,则0.1mol/L的Na2B溶液中,c(Na+)=2c(B2﹣)+2c(HB﹣)
H++B2﹣,则0.1mol/L的Na2B溶液中,c(Na+)=2c(B2﹣)+2c(HB﹣)
(6)25℃时Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20,
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33。在25℃下,向浓度均为0.1mol·L-1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式)。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+刚好完全沉淀时,测定c(Al3+)=0.2mol·L-1。此时所得沉淀中________(填“还含有”或“不含有”)Al(OH)3。