把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是
| A.H2SO4溶液 | B.Na2SO4溶液 | C.Na2CO3溶液 | D.FeC13溶液 |
关于图中四个图像的说法正确的是(注:图中,E表示能量,p表示压强,t表示时间,V表示体积,B%表示B的体积百分含量。) ( )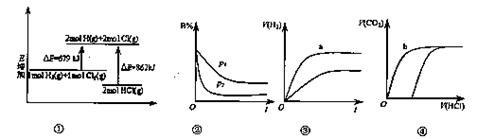
A.①表示化学反应H2(g)+Cl2(g) =2HCl(g)的能量变化,则该反应的反应热△H ="183" j/mol |
B.②表示其它条件不变时,反应4A(g)+3B(g) 2C(g)+6D在不同压强下B%随时间的变化,则D-定是气体 |
| C.③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D.④表示10 mL O.lmol/L NaCO3和NaHCO3两种溶液中,分别滴加0.lmol/L HCl产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
Na2S溶液中存在多种微粒,下列各微粒间的关系正确的是 ( )
| A.c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| B.c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| C.c(Na+)=c(HS-)+2c(H2S)+2c(S2-) |
| D.c(OH-)=c(H+)+c(HS-)+2c(H2S) |
以下盐溶液加热蒸干得不到原来的盐的是
A. Na2CO3 B. CuSO4 C. MgCl2 D KCl
广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法中不正确的是:
| A.CaO2的水解产物是Ca(OH)2和H2O2 | B.PCl3的水解产物是HClO和PH3 |
| C.NaClO的水解产物之一是HClO | D.Mg3N2的水解产物是两种碱性物质 |
在配制Al2(SO4)3溶液时,铝离子会部分水解而使溶液呈酸性,水解的离子方程式为: 。为了防止发生水解,可以加入少量的 ;在Na2S溶液中,硫离子水解的离子方程是 ;为了防止水解,在配制该溶液时,可以加入少量的 。
用物质的量都是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是 ( )
| A.c(H+)>c(OH-) |
| B.c(CH3COO-)+c(CH3COOH)=0.2 mol·L-1 |
| C.c(CH3COOH)>c(CH3COO-) |
| D.c(CH3COO-)+c(OH-)=0.1 mol·L-1 |
为了避免电解液中CuSO4因水解发生沉淀,正确的操作方法是 ( )
| A.稀释 | B.加稀硫酸 | C.加NaOH溶液 | D.加热 |
下列物质中能抑制水的电离且使溶液呈现出酸性的是:
| A.Na2CO3 | B.Al2(SO4)3 | C.K2SO4 | D.H2SO4 |
在配制Al2(SO4)3溶液时,为了防止发生水解,可加入少量的 ;在配制Na2S溶液时,为了防止发生水解,可加入少量的 ;把AlCl3溶液蒸干后再灼烧,最后得到的主要固体产物是 。其理由是(用化学方程式表示,)
、 。
某溶液中存在的离子有:S2-、HS-、OH-、Na+、H+,则下列有关对该溶液的叙述中不正确的是( )
| A.离子浓度可能是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| B.组成该溶液的溶质只能是Na2S或NaHS或两者的混合物 |
| C.该溶液可能呈中性,或碱性,或酸性 |
| D.离子物质的量的关系是2n(S2-)+n(HS-)+n(OH-)=n(Na+)+n(H+) |
下列溶液中各微粒的浓度关系正确的是
| A.等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) |
| B.0.2mol/L的NaHSO4溶液中:c(Na+)>c(SO42-)> c(H+) > c(OH-) |
C.向NH4HCO3溶液中滴加NaOH溶液至中性:c(NH4+)+c(Na+)= c (HCO3-)+c(CO32-) (HCO3-)+c(CO32-) |
| D.0.1 mol/L pH=9的NaNO2溶液中:c(Na+)>c(NO2-)>c(OH-) >c(H+) |