在CH3COONa溶液中,各离子的浓度由大到小排列顺序正确的是( )
| A.c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
已知H2S为弱酸,关于硫化氢水溶液,下列说法不正确的是( )
| A.常温下,pH小于7 |
| B.存在关系式:c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| C.25 ℃时,由水电离产生的c(H+)>1×10-7mol·L-1 |
| D.向溶液中加入少量NaOH固体,c(S2-)增大 |
在 溶液中,下列等量关系成立的是( )
溶液中,下列等量关系成立的是( )
| A.c(OH-)= c(H+)+c(HCO3-)+2c(H2CO3) |
| B.2c(Na+)= c(CO32-)+ c(HCO3-)+ c(H2CO3) |
| C.c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-) |
| D.c(Na+)="2" c(CO32-)+ c(HCO3-)+ c(H2CO3) |
300 mL某浓度的NaOH溶液中含有60 g溶质。现欲配制1 mol /L NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
| A.1∶4 | B.1∶5 | C.2∶1 | D.2∶3 |
有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。则A的相对分子质量是( )
A.29 |
B.29 |
C.29 |
D.29 |
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A.950 mL 111.2 g | B.500 mL 117 g |
| C.1 000 mL 117 g | D.任意规格 111.2 g |
25℃时,在0.1 mol·L-1的下列溶液中,微粒的物质的量浓度关系正确的是
| A.NH4Cl溶液中:c(NH4+)>c(Cl—)>c(H+)>c(OH-) |
B.NaHSO3溶液(呈酸性)中:c(Na+)>c(HSO )>c(SO )>c(SO )>c(H2SO3) )>c(H2SO3) |
| C.CH3COONa溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
D.Na2CO3溶液中:2c(Na+)=c(CO )+ c(HCO )+ c(HCO )+c(H2CO3) )+c(H2CO3) |
下列叙述正确的是
| A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)= c(NH4+) |
| B.pH = 3的醋酸溶液,稀释至10倍后pH = 4 |
| C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7 |
| D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-) 减小 |
下列方法能使电离平衡H2O H+ + OH-向右移动,且使溶液呈酸性的是
H+ + OH-向右移动,且使溶液呈酸性的是
| A.向水中加入少量硫酸铝固体 | B.向水中加入少量硫酸氢钠固体 |
| C.向水中加入少量碳酸钠固体 | D.将水加热到100℃,使水的pH=6 |
有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是
| A.两溶液中OH-离子浓度相同 | B.用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| C.两溶液溶质物质的量浓度相同 | D.加入等体积的水稀释后,它们的pH仍相等 |
常温下,取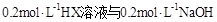 溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是
溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是
A.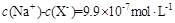 |
B.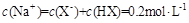 |
C. |
D.混合溶液中由水电离出的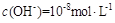 |
pH=a的某电解质溶液中,插入两支惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是 ( )
| A.NaOH | B.H2SO4 | C.AgNO3 | D.Na2SO4 |
用蒸馏水稀释1 mol/L醋酸时,始终保持增大趋势的是()
| A.溶液中的c(CH3COO-) | B.溶液中的c(H+) |
| C.溶液中的c(CH3COOH) | D.溶液中的c(OH-) |
对0.1 mol·L-1的醋酸溶液进行以下操作,下列分析判断正确的是()
| A.加入少量0.1 mol·L-1的硫酸,水电离产生的c(H+)减小 |
| B.升高温度,溶液的pH会增大 |
| C.加入少量固体NaOH,溶液中c(CH3COO-)+c(OH-)>c(Na+)+c(H+) |
| D.与0.1 mol·L-1的NaOH溶液等体积混合后,溶液中c(CH3COO-)=c(Na+) |
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH)="=" 0时,c(H+,W)="=" 1 × 10-2 mol/L |
B.V(NaOH)< 10 mL时,不可能存在c(Na+)="=" 2 c(C2O )+ c(HC2O )+ c(HC2O ) ) |
| C.V(NaOH)="=" 10 mL时,c(H+,W)="=" 1 × 10-7mol/L |
D.V(NaOH)> 10 mL时,c(Na+)> c(C2O )>c(HC2O )>c(HC2O ) ) |