CaH2常作为生氢剂,其中氢元素呈-1价,其化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑,其中水是( )
| A.还原剂 | B.氧化剂 |
| C.既是还原剂又是氧化剂 | D.既不是氧化剂又不是还原剂 |
下列化学反应中,属于氧化还原反应的是
| A.Na2CO3+CaCl2=CaCO3↓+2NaCl |
| B.2Cu+O2=2CuO |
| C.CaCO3+2HCl=H2O+CO2↑+CaCl2 |
| D.2H2+O2=2H2O |
已知:(1)H2(g)+H2O(g) ΔH1="a" kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g) ΔH2="b" kJ·mol-1
(3)H2(g)+=H2O(l) ΔH3="c" kJ·mol-1
(4)2H2(g)+O2(g)2H2O(l) ΔH4="d" kJ·mol-1
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
下列反应中气体作氧化剂的是
| A.S03通入水中:S03+H20=H2S04 |
| B.C12通人FeCl2溶液中:C12+2FeCl2=2FeCl3 |
| C.HCl通入NaOH溶液中:HCl+NaOH=NaCl+H20 |
| D.C02通入NaOH溶液中:C02+2NaOH=Na2C03+H20 |
下述反应①、②分别是从海藻灰和智利硝石中提取碘的主要反应:

根据上述信息,判断下列说法正确的是 ( )
| A.两个反应中NaHS04均为氧化产物 |
| B.在反应①中NaI是氧化剂,在反应②中NaI03中的碘元素被氧化 |
| C.氧化性:Mn02>SO42一>IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数之比为1:5 |
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少
量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是 ( )
| A.上述实验证明还原性:MnO-4>Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+H+,下列说法正确的是( )
| A.H2O2的氧化氢比Fe3+强,其还原性比Fe2+弱 |
| B.在H2O2分解过程中,溶液的pH逐渐下降 |
| C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变 |
| D.H2O2生产过程要严格避免混入Fe2+ |
R、X、Y和Z是四种元素,它们常见化合价均为+2,且X2+与单质R不反应;X2++Z===X+Z2+;Y+Z2+===Y2++Z。这四种离子被还原成0价时表现的氧化性大小符合
| A.R2+>X2+>Z2+>Y2+ | B.X2+>R2+>X2+>Z2+ |
| C.Y2+>Z2+>R2+>X2+ | D.Z2+>X2+>R2+>Y2+ |
判断氧的非金属性比硫强的事实是( )
| A.氢硫酸敞口放置于空气中变浑浊 |
| B.常温下Hg不与O2反应而与硫粉反应 |
| C.Fe在氧气中燃烧生成Fe3O4,而与硫反应生成FeS |
| D.氧的游离态大量存在于空气中;而硫的游离态主要存在于火山口喷口处 |
利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层深蓝色的Fe3O4(也可表示为FeFe2O4)薄膜,保护内部金属免受腐蚀,这种方法叫做烤蓝。烤蓝时发生如下反应: ① 3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
① 3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑ ② Na2FeO2+NaNO2+H2O—Na2Fe2O4+NH3↑+NaOH(未配平)
② Na2FeO2+NaNO2+H2O—Na2Fe2O4+NH3↑+NaOH(未配平) ③ Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
③ Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH 下列说法中正确的是
下列说法中正确的是
A.Fe3O4既可看作是氧化物,又可看作是亚铁盐  |
B.反应②配平后,H2O的化学计量数为3 |
C.反应③中,Na2Fe2O4是氧化剂,Na2FeO2是还原剂 |
D.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。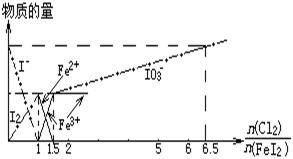
据此得出的下列结论中错误的是
| A.I-、Fe2+、I2的还原性和Cl2、Fe3+、I2的氧化性都依次减小 |
| B.当n(Cl2)/n(FeI2)==1.2时,离子方程式为2Fe2++10I-+6Cl2==5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)==6.5时,溶液中n(Cl-)/n(IO3-)==6.5 |
| D.若溶液体积不变,溶液的pH始终不变 |