根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是
①2Fe3++2I-=2Fe2++I2
②2Fe2++C12=2Fe3++2C1-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
| A.Fe3+>C12>MnO4- | B.Fe3+>Cl2>I2 |
| C.I2>Cl2>Fe3+ | D.MnO4->Cl2>Fe3+ |
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是( )
| A.既不是氧化剂也不是还原剂 | B.是氧化剂 |
| C.是还原剂 | D.既是氧化剂又是还原剂 |
下列变化必需加入氧化剂才能实现的是
| A.NH4+→NH3 | B.SO32-→SO42- | C.HNO3→NO | D.CO32-→CO2 |
X、Z、Y、W 均为四种金属, 根据下列事实:①X+Y2+=X2++Y;②Z+2H2O(冷水)=Z(OH)2+H2↑;③Z2+的氧化性比X2+弱;④由Y、W电极组成的原电池,电极反应为W2++2e-=W、Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为 ( )
| A.X﹥Z﹥Y﹥W | B.Z﹥W﹥X﹥Y |
| C.Z﹥Y﹥X﹥W | D.Z﹥X﹥Y﹥W |
已知:①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2﹣易被氯气氧化;④氯化氢比硫化氢稳定;⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应。上述叙述中可说明氯元素比硫元素非金属性强的是( )
| A.①②③ | B.②③④ | C.③④⑤ | D.①③⑤ |
制备单质硅时,主要化学反应如下
①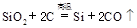 ②
② ③
③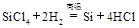 下列对上述三个反应的叙述中,不正确的是( )
下列对上述三个反应的叙述中,不正确的是( )
| A.①③为置换反应 | B.①②③均为氧化还原反应 |
| C.②为化合反应 | D.三个反应的反应物中硅元素均被氧化 |
科技工作者研究出以NH3为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示)。该固体氧化物电解质的工作温度高达700~900 ℃,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是
| A.电极甲为电池正极 |
| B.电池总反应为4NH3+5O2=4NO+6H2O |
| C.电池正极反应式为O2+2H2O+4e-=4OH- |
| D.图示中的O2-由电极乙移向电极甲 |
从海水中提取溴的过程中涉及到反应:Br2 + SO2 + 2H2O =" 2HBr" + H2SO4,下列说法正确的是
| A.Br2在反应中被氧化 |
| B.SO2在反应中表现还原性 |
| C.H2SO4是还原产物 |
| D.1 mol氧化剂在反应中失去2 mol电子 |
下列各反应中,水作为还原剂的是( )
A.2H2+O2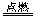 2H2O 2H2O |
B.SO3+H2O==H2SO4 |
| C.2F2+2H2O==4HF+O2 | D.2Na+2H2O==2NaOH+H2 ↑ |
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 | B.工业和生活中常用HF来刻蚀玻璃 |
| C.工业上利用合成氨实现人工固氮 | D.工业上电解熔融状态Al2O3制备Al |
甲乙两种非金属:①甲比乙容易与H2化合;②甲的氢化物比乙的氢化物稳定③
甲的最高价氧化物对应的水化物的酸性比乙的最高价氧化物对应的水化物酸性强;
④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低。能说
明甲比乙的非金属性强的是
| A.只要④ | B.只有⑤ | C.①②③④⑤ | D.①②③ |
根据下列实验事实:
(1)X+Y2+===X2++Y (2)Z+2H2O Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+的氧化性比X2+弱 (4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是( )
| A.X>Y>Z>W | B.Y>X>W>Z | C.Z>X>Y>W | D.Z>Y>X>W |