从海带灰中可以提取碘,主要反应为:Cl2+2I- I2+2Cl-,下列说法不正确的是
I2+2Cl-,下列说法不正确的是
| A.该反应属于置换反应 | B.反应中I-离子发生还原反应 |
| C.Cl2的氧化性比I2的氧化性强 | D.生成1mol I2转移2mol e- |
若某溶液中有Fe2+和I-共存,要氧化I-而又不氧化Fe2+,可加入的试剂是
| A.Cl2 | B.KMnO4 |
C.HCl | D.FeCl3 |
在反应中3S+6KOH =2K2S+ K2SO3+3H2O,氧化剂与还原剂的质量之比是
| A.1∶2 | B.2∶1 | C.1∶1 | D.3∶2 |
已知在适宜的条件下发生如下反应:①C+CO2=2CO ②C+H2O=CO+H2 ③CO +H2O=CO2+H2由此可以判断,在该温度下,C、CO、H2的还原性强弱顺序是
A.CO>C>H2 B.C>CO>H2 C.C>H2>CO D.CO>H2>C
下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是
| A.在氧化-还原反应中,甲原子失去的电子比乙原子失去的电子多 |
| B.同价态的阳离子,甲比乙的氧化性强 |
| C.甲能跟稀盐酸反应放出氢气而乙不能 |
| D.将甲、乙作电极组成原电池时,甲是正极 |
关于反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O的叙述中,正确的是
| A.KCl中含有35Cl | B.生成物Cl2的相对分子质量为73.3 |
| C.该反应转移的电子数为6e- | D.氧化剂和还原剂的物质的量之比为1:6 |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为a HClO3 = bO2↑+ c Cl2↑+ d HCl O4 + e H2O。下列有关说法不正确的是
O4 + e H2O。下列有关说法不正确的是
| A.由反应可确定:氧化性HClO3>O2 |
B.由非 金属性Cl>S,可推知酸性HClO3>H2SO4 金属性Cl>S,可推知酸性HClO3>H2SO4 |
| C.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液加入溴水后,溴被还原,由此推断该溶液中
| A.不含NO3-,也不含Fe3+ | B.含有NO3-、I-、Cl- |
| C.含I-,不含Cl- | D.含有Fe3+ |
把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。上述一系列过程中,最终被还原的是
| A.SO2 | B.Cl- | C.Fe3+ | D.NO |
下列变化,必须要加入氧化剂才能实现的是
| A. HCl→H2 | B. H2O2→O2 | C. H2SO4→SO2 | D. Fe→Fe3O4 |
对反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是( )
| A.该反应的氧化剂只有CuSO4 |
| B.SO42﹣既不是氧化产物也不是还原产物 |
C.1molCuSO4氧化了 mol的S mol的S |
| D.被还原的S和被氧化的S的质量比为3:7 |
下列比较中,正确的是
| A.原子半径:Na>Mg | B.碱性:NaOH>KOH |
| C.结合H+的能力:CO32¯<Cl¯ | D.还原性:I¯<Br¯ |
已知在酸性溶液中的还原性强弱顺序为:SO2 > I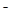 > H2O2 > Fe
> H2O2 > Fe > Cl
> Cl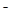 ,下列反应不可能发生的是
,下列反应不可能发生的是
A.2I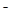 + Fe + Fe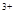 =I2 + Fe =I2 + Fe |
B.2Fe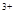 + SO2 + 2H2O=2Fe + SO2 + 2H2O=2Fe + SO + SO + 4H+ + 4H+ |
| C.SO2 + 2H2O + I2=H2SO4 + 2HI |
| D.H2O2 + H2SO4=SO2↑ + O2↑ + 2H2O |