常用的电池是一个液体电解质将两个固体电极隔开。而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过。下列有关说法不正确的是
| A.a为电池的正极 |
| B.充电时b接电源的正极 |
| C.正极反应为:nS8+16ne-=8Sn2- |
| D.Na+可以穿过固体电解质从而传递电流 |
(14分)甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2加氢合成甲醇是合理利用CO2的有效途径。由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g)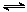 CH3OH(g) +H2O(g) △H 1=-49.58kJ•mol-1
CH3OH(g) +H2O(g) △H 1=-49.58kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)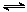 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2 H2(g)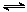 CH3OH(g) △H 3=-90.77 kJ•mol-1
CH3OH(g) △H 3=-90.77 kJ•mol-1
回答下列问题:
(1)反应Ⅱ的△H2= ,反应I自发进行条件是 (填“较低温”、“较高温”或“任何温度”)。
(2)在一定条件下3L恒容密闭容器中,充入一定量的H2和CO2仅发生反应Ⅰ,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线,如图1所示。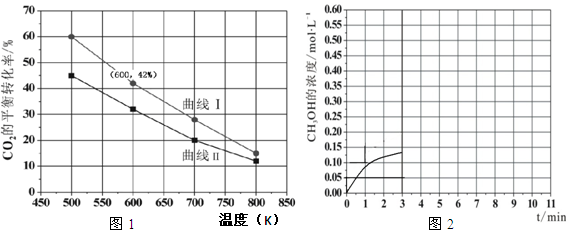
①H2和CO2的起始的投入量以A和B两种方式投入
A:n(H2)=3mol,n(CO2)=1.5mol
B:n(H2)=3mol,n(CO2)=2mol,曲线I代表哪种投入方式 (用A、B表示)
②在温度为500K的条件下,按照A方式充入3mol H2和1.5mol CO2,该反应10min时达到平衡:
a.此温度下的平衡常数为 ;500K时,若在此容器中开始充入0.3molH2和0.9mol CO2、0.6molCH3OH、xmolH2O,若使反应在开始时正向进行,则x应满足的条件是
b.在此条件下,系统中CH3OH的浓度随反应时间的变化趋势如图2所示,当反应时间达到3min时,迅速将体系温度升至600K,请在图2中画出3~10min内容器中CH3OH浓度的变化趋势曲线。
(3)固体氧化物燃料电池是一种新型的燃料电池,它是以固体氧化锆、氧化钇为电解质,这种固体电解质在高温下允许氧离子(O 2-)在其间通过,该电池的工作原理如下图所示,其中多孔电极均不参与电极反应,下图是甲醇燃料电池的模型。
①出该燃料电池的负极反应式
②如果用该电池作为电解装置,当有16g甲醇发生反应时,则理论上提供的电量最多为 (法拉第常数为9.65×104C·mol-1)
已知外电路中,电子由铜流向a极。有关下图所示装置的分析中,合理的一项是
| A.一段时间后Zn电极逐渐溶解 |
| B.该装置中Cu极为正极,发生还原反应 |
| C.b极反应的电极反应式为:H2-2e-=2H+ |
D.电流方向: |
一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构结构如下图:

以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s)+ Cu2+(aq)= Zn2+ + Cu(s) △H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是
C6+LiCoO2。下列说法不正确的是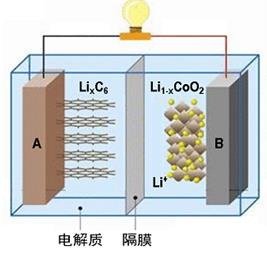
| A.据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边流向右边 |
| B.放电时,正极锂的化合价未发生改变 |
| C.充电时B作阳极,该电极放电时的电极反应式为:Li1-x CoO2+ xLi++ xe-= LiCoO2 |
| D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收 |
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是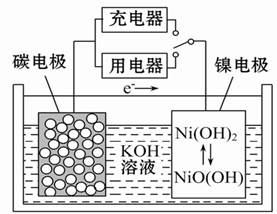
| A.放电时,OH-向镍电极作定向移动 |
| B.放电时,负极的电极反应为:H2-2e-+2OH-="==" 2H2O |
| C.充电时,将电池的碳电极与外电源的正极相连 |
| D.充电时,阴极的电极反应为:Ni(OH)2+OH--e-===NiO(OH)+H2O |
(16分)运用化学原理知识研究化学对于人类的生产生活、科研意义重大。
(1)工业上以黄铜矿(主要成分:CuFeS2,其中S为-2价)为原料,采用火法熔炼工艺生产粗铜。CuFeS2中Fe的化合价为_____,熔炼过程中所得炉渣的主要成分有FeO、Fe2O3、SiO2,Al2O3等,若要利用炉渣制取铁红,下列实验操作不需要的是_____(填写字母代号)。
| A.溶解 | B.过滤 | C.蒸发结晶 | D.灼烧 |
(2)Mg(OH)2是水垢的主要成分之一,用氯化铵溶液浸泡:可以溶解Mg(OH)2,请结合平衡移动原理解释其原因_____。
(3)研究发现CuCl2溶液中铜、氯元素的存在形式为Cu(H2O)42+、CuCl42-,电解CuCl2溶液一段时间,阳极产生2.24L(标准状况)黄绿色气体,阴极析出红色物质,试计算该过程中共转移电子____mol,若要使电解质溶液恢复至原浓度,应向电解后的溶液中加入________。
(4)以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2。其工作原理如图所示。电池放电时Na+由____(填写“a”或“b”,下同)极区移向___________极区,该电池的负极反应式为__________________________________。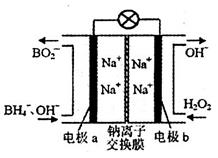
液流电池是一种新的蓄电池,是利用正负极电解液分开,各自循环的一种高性能蓄电池,具有容量高、使用领域(环境)广、循环使用寿命长的特点。如图是一种锌溴液流电池,电解液为溴化锌的水溶液。下列说法正确的是
A.充电时阳极的电极反应式:Zn-2e-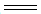 Zn2+ Zn2+ |
| B.充电时电极a为外接电源的负极 |
| C.放电时Br-向右侧电极移动 |
| D.放电时左右两侧电解质储罐中的离子总浓度均增大 |
利用人工模拟光合作用合成甲酸的原理为:
2CO2+2H2O 2HCOOH+O2,装置如图所示,
2HCOOH+O2,装置如图所示,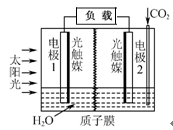
下列说法不正确的是
| A.电极1周围pH增大 |
| B.电子由电极1经过负载流向电极2 |
| C.电极2的反应式:CO2+2H++2e-=HCOOH |
| D.该装置能将太阳能转化为化学能和电能 |
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。
(1)工业上正在研究利用CO2来生产甲醇燃料的方法。
已知:H2(g)+1/2O2(g)===H2O(g)ΔH1=-242 kJ/mol
CH3OH(g)+3/2O2(g)===CO2(g)+2H2O(g) ΔH2=-676 kJ/mol
①写出CO2和H2反应生成气态甲醇等产物的热化学方程式:___________________。
②下面表示合成甲醇的反应的能量变化示意图,其中正确的是________(填字母序号)。
(2)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
①该电池外电路电子的流动方向为________(填写“从A到B”或“从B到A”)。
②工作结束后,B电极室溶液的酸性与工作前相比将________(填写“增大”、“减小”或“不变”,溶液体积变化忽略不计)。
③A电极附近甲醇发生的电极反应式为________。
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如下图所示。下列说法不正确的是
| A.该系统中不只存在化学能和电能的相互转化 |
B.在移位反应器中,反应CO(g)+H2O(g)  CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 |
| C.改质器和移位反应器的作用是将CxHy转化为H2和CO2 |
| D.该电池正极的电极反应为O2+4H+—4e-===2H2O |
某科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半。他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料,与电 解质和正极材料(石墨)构成可充电电池。若电解液为LiAlCl4-SOCl2,电池的总反应为:
4LiCl+S+SO2 4Li+2SOCl2
4Li+2SOCl2
下列说法正确的是
| A.电池的电解液可为LiCl水溶液 |
| B.放电时负极反应式为:Li-e-+ Cl-=LiCl |
| C.放电时正极反应式为: 2SOCl2+4e-=4Cl-+S+SO2 |
| D.放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
某课外活动小组设想:如果模拟工业上离子交换膜法制烧碱的方法,利用下图实验装置(两电极均为石墨电极)电解 溶液来制取
溶液来制取 、
、 、
、 和NaOH,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
和NaOH,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
(1)该电解槽的阳极反应式为 ,此时通过阴离子交换膜的离子数 (填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
(2)制得的 溶液从出口 (填“A”、“B”、“C”或“D”)导出。
溶液从出口 (填“A”、“B”、“C”或“D”)导出。
(3)利用制得的氢气为基本原料合成出甲醇,然后再用甲醇与氧气、氢氧化钠组成燃料电池,则该电池负极的电极反应式为 。
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
A.该电池的负极反应为   |
| B.电池放电时Na+从b极区移向a极区 |
| C.每消耗3 mol H2O2,转移的电子为3 mol |
| D.电极a采用MnO2作电极材料 |
铅蓄电池用途极广,电解液为30% H2SO4溶液,电池的总反应式可表示为:Pb(s)+PbO2(s)+2H2SO4(aq)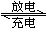 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
下列有关叙述正确的是
| A.放电时电解液的密度不断增大 |
| B.放电时电子从Pb通过导线转移到PbO2 |
| C.充电时Pb极与外电源的负极相连 |
| D.充电时PbO2电极发生还原反应,Pb电极上发生氧化反应 |