Li-I2 电池广泛用于笔记本电脑、摄像机等,下列有关锂电池工作原理的说法中不正确的是
| A.锂在反应中被还原 | B.该电池总反应式为:2Li+I2=2LiI |
| C.锂电池是一种高能电池 | D.正极的电极反应式为:I2+2e-=2I- |
目前市场上主流手机所配的电池基本上都是锂离子电池。它的负极材料是金属锂和碳的复合材料,组成为C6Li,其中碳作为金属锂的载体,电解质为一种能传导Li+的有机导体或高分子材料。这种锂离子电池的电池反应式为:0.45Li+Li0.56CoO2 LiCoO2下列说法不正确的是 ( )
LiCoO2下列说法不正确的是 ( )
| A.放电时电池内部Li+向负极移动 |
| B.该电池不能选用水做溶剂的电解质 |
| C.放电时,正极的电极反应式:0.45Li++Li0。55CoO2+0.45e- |
| D.充电时,外接电源的正极与电池上标注“+”的电极连接 |
下列说法不正确的是 ( )
| A.与铜质水龙头连接处的钢制水管易发生腐蚀 |
| B.把被保护的钢铁设备作为阴极,外加直流电源可进行保护 |
| C.原电池产生电流时,阳离子移向正极,阴离子移向负极 |
| D.铅蓄电池是最常见的二次电池,正极板上覆盖有Pb |
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4 = 2PbSO4+2H2O,下列有关说法正确的是
| A.图中涉及的能量转化方式只有3种 |
| B.蓄电池供电时,负极的电极反应为:Pb +SO42―-2e-=PbSO4 |
| C.储能时若充电时间过长,阳极流向阴极的气体可能是H2 |
| D.该发电工艺可实现零排放 |
芬兰籍华人科学家张霞昌研制的“超薄型软电池”获2009年中国科技创业大赛最高奖,被称之为“软电池”的纸质电池总反应为:Zn + 2MnO2 + H2O ="=" ZnO + 2MnO(OH)(碱式氧化锰)。下列说法正确的是 ( )
| A.该电池中Zn作负极,发生还原反应 |
| B.该电池反应中MnO2起催化作用 |
| C.该电池工作时电流由Zn经导线流向MnO2 |
| D.该电池正极反应式为:2MnO2 + 2e- + 2H2O ="=" 2MnO(OH)+ 2OH- |
氢氧燃料电池的基本构造如图。A、B是多孔石墨制成,通入的气体由孔隙中逸出,在电极表面得失电子。电解质溶液是KOH溶液。下列关于该电池的说法中错误的是
A.H2发生氧化反应 B.e-由B电极流向A电极
C.A电极为负极 D.每摩O2得到4mole-
下图是一种航天器能量储存系统原理示意图。下列说法正确的是
| A.该系统中只存在3种形式的能量转化 |
B.装置Y中负极的电极反应式为: |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现 |
化学能与电能间的完全转化
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁—过氧化氢燃料电池系统。其工作原理如图所示。以下说法中错误的是
| A.电池的负极反应为:Mg – 2e-= Mg2+ |
| B.电池工作时,H+向负极移动 |
| C.电池工作一段时间后,溶液的pH增大 |
| D.电池总反应是:Mg + H2O2 + 2H+= Mg2++ 2H2O |
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O;7H2O+7/2O2+14e-=14OH-。有关此电池的推断正确的是
| A.通氧气的电极为负极 |
| B.参加反应的O2与C2H6的物质的量之比为7∶2 |
| C.电池工作一段时间后,KOH的物质的量浓度不变 |
| D.电池工作时,溶液中OH-离子向正极移动 |
据报道,锌电池可能取代目前广泛应用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为:2Zn+02=2ZnO,原料为锌粒、电解质和空气,则下列叙述正确的是
| A.锌为正极,空气进入负极反应 | B.负极反应为Zn-2e-=Zn2+ |
| C.正极发生氧化反应 | D.电解液肯定是强酸 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以KOH溶液为电解液,电池总反应式为:Zn(s) + 2MnO2(s) + H2O(l)===Zn(OH)2(s) + Mn2O3(s)。下列说法正确的是( )
| A.该电池的正极为锌 |
| B.电池正极的反应式为:2MnO2(s) + H2O(1) + 2e— ="==" Mn2O3(s) + 2OH—(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.该电池反应中二氧化锰起催化作用 |
氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2 + O2 = 2H2O,正极反应为:O2 + 2H2O + 4e- = 4OH-下列叙述不正确的是
| A.H2通入负极区 | B.O2通入正极区 |
| C.负极反应为2H2 + 4OH- — 4e- = 4H2O | D.正极发生氧化反应 |
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(下图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。

甲 乙
下列有关叙述正确的的是
| A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| B.电极b是正极,O2-由电极a流向电极b |
| C.电极a的反应式为:CH4+4O2—―8e-=CO2 +2H2O |
| D.当固体电解质中有1 mol O2-通过时,电子转移4mol |
下图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气 体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是
体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是 
| A.该电池工作过程中,H+浓度不断增大 |
| B.该电池在高温环境下能提供更好的动力 |
| C.该电池负极反应为:H2—2e—=2H+ |
| D.该电池正极反应为O2+4e—=2O2- |
如下图所示,用铅蓄电池电解100g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5g。下列说法正确的是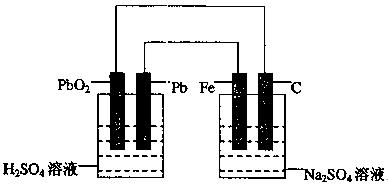
| A.电路中转移0.25mol电子 |
| B.铅蓄电池中消耗0.5mol H2SO4 |
| C.铅蓄电池的负极反应式为:PbSO4+2H2O—2e-=PbO2+4H++SO2-4 |
| D.Fe电极发生的电极反应为Fe—2e-=Fe2+ |