废电池造成污染的问题日益受到关注,集中处理废电池的首要目的是
| A.回收石墨电极 |
| B.回收电池外壳的金属材料 |
| C.防止电池中渗泄的电解液腐蚀其他物品 |
| D.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
镍铬(Ni-Cd)可充电电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:
Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和
Cd(OH)2 + 2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和
NiOOH都不溶于KOH溶液。则下列有关电极反应式正确的是
| A.放电时负极:Cd-2e-=Cd2+ |
| B.放电时正极:2NiOOH + 2e- + 2H2O=2Ni(OH)2 + 2OH- |
| C.充电时阳极:2Ni(OH)2-2e-+ 4H+=2Ni3+ + 4H2O |
| D.充电时阴极:Cd(OH)2 + 2e-=Cd + 2OH- |
燃料电池是利用燃料(如H2、CO、CH4等)跟氧气反应从而将化学能转化成电能的装置。下列关于甲烷燃料电池(NaOH溶液作电解质)的说法中正确的是
| A.负极反应为:O2+2H2O+ 4e-= 4OH- |
| B.负极反应为:CH4+ 10OH-- 8e-= CO32- + 7H2O |
| C.放电时正极发生氧化反应,外电路中电子从正极流向负极 |
| D.随着放电的进行,溶液的pH保持不变 |
一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH + 3O2 =" 2" CO2 + 3H2O,电池构造如下图。下列关于该电池的说法不正确的是
| A.放电过程中,电源内部的H+从正极区向负极区迁移 |
| B.通入乙醇的电极是负极 |
| C.该电池的正极反应为:4H+ + O2 + 4e-= 2H2O |
| D.用该电池做为电源,用惰性电极电解饱和NaCl的水溶液时,每消耗0.2 mol C2H5OH,阳极产生标准状况下气体的体积为26.88 L |
Al-AgO 电池性能优越,可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是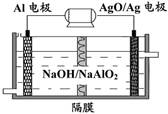
| A.AgO/Ag电极是负极 |
| B.当电极上析出1.08 g Ag时,电路中转移的电子为0.02mol |
| C.Al电极的反应式为:Al—3e-+4OH-= AlO2-+2H2O |
| D.在电解质溶液中OH-由Al电极移向AgO/Ag电极 |
已知铅蓄电池放电过程可以表示为PbO2 + 2 H2SO4 + Pb="2" PbSO4 + 2H2O下列关于铅蓄电池的说法正确的是
| A.Pb为正极,PbO2为负极 |
| B.正极电极反应式为PbO2 + SO4 2- + 2H+ =PbSO4 + H2O |
| C.硫酸溶液中,H+移向负极 |
| D.放电一段时间后,SO4 2-浓度减小 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是( )
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
下列说法不正确的是
| A. | 多孔碳可用作氢氧燃料电池的电极材料 |
| B. |
|
| C. |
科学家发现一种新细菌的
|
| D. |
 和 和
 ,反应符合绿色化学的原则 ,反应符合绿色化学的原则
|
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱 |
| D.电池正极的正极反应为4H++O2+4e-=2H2O |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池工作时,电子由正极通过外电路流向负极 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq) |
| D.外电路中每通过O.2mol e-,锌的质量理论上减小6.5g |
将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是:CH4+10OH--8e-=CO32- +7H2O;通入O2的另一极,其电极反应式是:2O2+4H2O+8e-=8OH-。下列叙述不正确的是( )
| A.通入CH4的电极为负极 | B.正极发生氧化反应 |
| C.燃料电池工作时,溶液中的OH-向负极移动 | D.该电池使用一段时间后应补充KOH |
已知空气—锌电池的电极反应为
锌片:Zn+2OH――2e-=ZnO+H2O;
碳棒:O2+2H2O+4e- =4OH- ,据此判断,锌片是
| A.正极,被还原 | B.正极,被氧化 |
| C.负极,被还原 | D.负极,被氧化 |