在短周期元素中:①金属性最强的元素是______,与水反应最剧烈的非金属是_____;②地壳中含量最丰富的元素位于第________周期第________族,地壳中含量最多的金属元素位于周期表的第________周期第________族.
在11~18号的元素中,③原子半径最小的元素是________;④元素最高价氧化物中既能与盐酸反应又能与烧碱反应,该氧化物是________.
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a  b
b  c
c 
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特 点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。
A、B、C、 D、E都是原子序数依次增大的五种短周期元素,已知:
①A和 C属同族元素,且A元素的原子半径是短周期元素原子中半径最小的;
②A和B能形成组成为A2B和A2B2的两种化合物;
③D元素原子所形成的离子在同周期元素原子形成的离子中半径是最小的;且D元素原子的最外层电子数是E元素原子最外层电子数的一半。
请回答:
(1)A元素是________;C元素是_________。D元素是_________。E元素是_________。(填元素符号)
(2)化合物A2B2的所含化学键______________电子式是____________;
(3)B和E形成两种常见化合物是_________和_________。
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。
请回答下列问题:
(1)这些元素的氢化物中,水溶液碱性最强的是________(写化学式),该氢化物的电子式为________。
(2)元素X和元素Y的最高价氧化物对应水化物的酸性较弱的是________,列举一个化学方程式证明________________________。
(3)元素Z与元素M组成的化合物中所含化学键类型为________,元素Z与元素X组成的化合物中所含化学键类型为________。
(1)同一短周期元素的电子层数__________,但随着原子序数的递增,最外层电子数逐渐__________、原子半径逐渐___________,因此失电子能力逐渐__________,得电子能力逐渐_________,所以元素的金属性逐渐___________,非金属性逐渐___________。 第三周期非金属元素的最高价氧化物的水化物酸性由强到弱的顺序是________________________________________。
(2)日常生活中用于减缓食物腐败变质的措施和方法有__________________________、
________________________________、____________________________________等。
A、B、C、D、E、F、G是元素周期表前四周期的元素,它们在元素周期中的位置如下图所示:
⑴写出G的基态原子核外电子排布式:__________________。
⑵B元素氢化物接近沸点的蒸气的相对分子质量测定值比用化学式计算 出来的相对分子质量大一些,其原因是: 。
出来的相对分子质量大一些,其原因是: 。
⑶EB晶胞如右图所示,EB晶体中E2+的配位数为 ,EB晶体
和NaCl晶体中离子排列方式相同,其晶格能分别为:
EB-3401kJ/mol、NaCl-786kJ/mol。导致两者晶格能差异的主要
原因是_______________________________________________。
⑷请用原子结构的知识解释检验D元素时焰色反应产生的现象的原因是 
在 H,
H, H,
H, H,
H, Mg,
Mg, Mg,
Mg, O,
O, O,
O, O中共有______种元素,______种原子,中子数最多的是 。D218O的相对分子质量是______。
O中共有______种元素,______种原子,中子数最多的是 。D218O的相对分子质量是______。
利用周期表中同族元素的相似性,可预测元素的性质。
(1)P元素的基态原子有_______个未成对电子,白磷的分子式为P4,其结构如下图所示。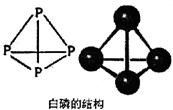
科学家目前合成了N4分子,N原子的杂化轨道类型是________,N -N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途为________。
(2) N、P、As原子的第一电离能由大到小的顺序为________。
(3)立方氮化硼晶体的结构如下图所示:
该晶体中,B原子填充在N原子的________空隙,且占据此类空隙的比例为________ (填百分数)。
(4) N与As是同族元素,B与Ga是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是________;立方砷化镓晶体的晶胞边长为a pm,则其密度为________g·cm-3 (用含a的式子表示,设NA为阿伏加德罗常数的值)。
填空题
(1)碳原子最外电子层含有__________个电子,一个碳原子可以跟其他非金属原子形成__________共价键。
(2)在有机合成过程中,引入碳碳双键的三种方法是_____________、________________、_____________。
(3)根据官能团不同,单糖可分为_______________和________________________。
(4)核酸分为DNA和RNA,DNA的主要功能是________________;RNA的主要功能是____________。
周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子;R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;X基态原子s能级的总电子数比p能级的总电子数多1;Y原子的核外成对电子数是未成对电子数的3倍;Z原子的价电子排布为3d74S2。
回答下列问题:
(1)R、X、Y中第一电离能最大的是 (填元素符号),其中Y原子的电子排布式为 。
(2)Q、R元素形成的某分子中共有14个电子,该分子中R原子采取 杂化,该分子的立体构型为 。
(3)RY可以和很多过渡金属形成配合物,如Fe( RY)5、Ni(RY)4。其中Fe(RY)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe (RY)5晶体属于 (填晶体类型)。RY与N2互为等电子体,与RY互为等电子体的离子有 (任写一种)。
(4)向含Z2+的溶液中加入过量的氨水,并通入适量的Y2气体,生成有[Z(NH3)6]3+离子,则该反应的离子方程式为 。
已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如下图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。(某些产物可能略去)
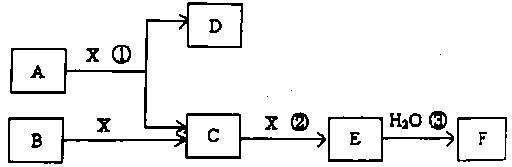
请回答下列问题:
(1)若E是有色气体,F是一元强酸,反应①是工业制备F的第一步反应。
①写出A与X反应的化学方程式: 。
②A的分子结构模型为 。
③已知常温下46g气体E发生反应③放出46kJ热量,写出气体E与H2O反应的热化学方程式 。
④在常温下,向V1LpH=a的A溶液中加入V2LpH=b的盐酸,且a+b=14,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(填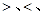 无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是 。(写出一种情况即可)
无法确定),所得溶液中各种离子的浓度由大到小的顺序可能是 。(写出一种情况即可)
(2)若E为无色无味气体,F是二元弱酸。
①E的电子式为 ;
②将少量气体E通入氢氧化钡溶液中得不溶物H,H的Ksp=8.1×10—9。现将该沉淀放入0.1mol/L的BaCl2溶液中,其Ksp ,(填:增大、减小或不变),此时,组成不溶物H的阴离子在溶液中的浓度为 mol/L。
原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M最外层电子数是电子层数的2倍,,N2+核外3d有9个电子,请回答下列问题:
(1)N位于元素周期表的 区,X、Y、Z的电负性最大的为 。
(2)XZ 中中心原子杂化方式为 。
中中心原子杂化方式为 。
(3) Z的氢化物(H2Z)在乙醇中的溶解度大于H2M,其原因是 。
(4)Na2M2Z3还原性较强,在溶液中易被Cl2氧化成MZ ,常用作脱氯剂,该反应的离子方程式为 。
,常用作脱氯剂,该反应的离子方程式为 。
(5)N与Y可形成的一种具有良好的电学和光学性能的化合物,其晶胞结构如图所示,则该化合物的化学式为 。
( 7分 )同一周期的主族元素,从左到右,原子半径逐渐 ,得电子能力逐渐______,非金属性逐渐______;同一主族元素,从上到下原子半径逐渐 ,失电子能力逐渐______,单质的还原性逐渐______,氧化性逐渐______。
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
①ⅡA族元素的价电子数 。
②第三周期元素的最高化合价 。
③F-、Na+、Mg2+、Al3+的离子半径 。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物对应的水化物的化学式为 。
②X、Y、Z元素符号分别为:X 、Y 、Z 。
③工业上制取单质M的化学方程式为_____________________________ 。
A、B、C、D、E是除稀有气体以外的5种短周期元素,原子序数依次增大并分占三个周期。B、C、D为同一周期依次相邻的3种元素,B和D的原子序数之比为3:4,E原子的电子层数等于最外层电子数。请回答相关问题:
(1)B元素在周期表中的位置 ,C元素是 (填元素符号)
(2)比较D和E简单离子半径大小(用离子符号表示): 。
(3)A与D形成含18电子化合物的化学式为 。
(4)元素E形成的简单离子的水溶液与c的氢化物的水溶液反应的离子方 程式
程式
 ;
;
(5)2007年7月2日,美、德两国科学家成功 合成了具有独特化学特性的E2A6化合物,该物质在D2中能烧,写出它在D2中完全燃烧的化学方程式 .
合成了具有独特化学特性的E2A6化合物,该物质在D2中能烧,写出它在D2中完全燃烧的化学方程式 .