如右图所示,锥形瓶中盛有气体X,滴管内盛有液体Y。若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
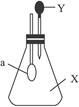
| A.X是NH3,Y是水 |
| B.X是SO2,Y是NaOH浓溶液 |
| C.X是CO2,Y是稀H2SO4 |
| D.X是HCl,Y是NaNO3稀溶液 |
已知硫氰(SCN)2、氰气(CN)2和Cl2性质相似。试完成下列反应:
(1)(CN)2+NaOH→___________________________________________________________。
(2)MnO2+HSCN→
_____________________________________________________________。
下列溶液中加入氯化钡溶液生成白色沉淀,在加入稀硝酸震荡,白色沉淀不消失的是
| A.Na2SiO3 | B.Na2CO3 | C.Na2SO3 | D.Na3PO4 |
把7.4gNa2CO3·10H2O和NaHCO3组成的混合物溶于水,配成100mLD 溶液,其中c(Na+)=0.6mol/L.若把等质量的混合物加热到恒重时,残留物的质量是( )
| A.3.18g | B.2.21g | C.5.28g | D.4.22g |
强热条件下,硫酸亚铁固体发生分解:2FeSO4=Fe2O3+SO2↑+SO3↑,如将此反应生成的气体通入BaCl2溶液中,则( )
| A.析出BaSO3沉淀 | B.析出BaSO4沉淀 |
| C.逸出SO3气体 | D.逸出SO2气体 |
如图所示,在火棉胶袋(半透膜)内注入淀粉和食盐溶液,用线系紧密封,使细玻管内的液面刚好高出烧杯内蒸馏水的液面,过一段时间后用碘酒和硝酸银溶液分别检验蒸馏水。整个实验过程中,所观察到的现象是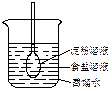
| A.细玻管内液面上升 | B.细玻管内液面不变 |
| C.蒸馏水遇碘酒变蓝 | D.蒸馏水遇硝酸银溶液有白色沉淀生成 |
将淀粉碘化钾混合溶液装在羊皮纸制成的袋中,将此袋下半部浸泡在盛有蒸馏水的烧杯里,过一段时间后取烧杯中液体进行实验,下列现象能证明羊皮袋一定有破损的是
| A.加入碘水变蓝色 |
| B.加入NaI溶液不变蓝色 |
| C.加入AgNO3溶液产生黄色沉淀 |
| D.加入溴水变蓝色 |
下列说法正确的是( )
| A.第ⅥIA族元素从上到下,其氢化物的还原性依次减弱 |
| B.同周期从左到右,非金属元素最高价氧化物对应的水化物的酸性依次增强 |
| C.第三周期元素的离子半径从左到右逐渐减小 |
| D.CCl4属于共价化合物,每个原子都满足8电子结构,其水溶液能导电 |
一定条件下,RO和氟气可发生如下反应:RO+F2+2OH-===RO+2F-+H2O从而可知在RO中,元素R的化合价是
| A.+4 | B.+5 | C.+6 | D.+7 |
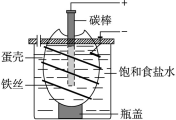
电解饱和食盐水简易装置
38.4 g铜跟适量的浓硝酸反应,铜全部作用后,共收集到气体22.4 L(标准状况下,不考虑N2O4),则反应消耗的硝酸的物质的量是
| A.1.0 mol |
| B.1.6 mol |
| C.2.2 mol |
| D.2.4 mol |
有Na2CO3、AgNO3、BaCl2、HCl及NH4NO3的无标签溶液,为鉴别它们,取四支试管分别装入一种溶液,向上述四支试管中加入少许剩下的一种溶液,下列结论错误的是
| A.有三支试管出现沉淀时,则后加入的是AgNO3溶液 |
| B.全部若没有什么现象变化时,则后加的是NH4NO3溶液 |
| C.一支试管出现气体,两支试管出现沉淀时,最后加入的是HCl溶液 |
| D.若只有两支试管出现沉淀时,则最后加入的是BaCl2溶液 |
现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是
①观察颜色 ②石蕊试剂 ③品红溶液
| A.只有①② |
| B.只有①③ |
| C.只有②③ |
| D.①②③ |
下列过程最终无沉淀产生的是
| A.过量氨气通入Al2(SO4)3溶液 |
| B.CO2通入CaCl2溶液 |
| C.少量SO2通入BaCl2溶液后再通入过量Cl2 |
| D.过量CO2通入Na2SiO3溶液 |
对于反应:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O,下列有关说法中不正确的是
| A.HNO3在反应中既表现氧化性也表现出酸性 |
| B.每生成22.4L NO(标准状况)有3mol电子转移 |
| C.HNO3作氧化剂,铜作还原剂,3molCu还原8 mol的HNO3 |
| D.HNO3作氧化剂,铜作还原剂,3molCu还原2 mol的HNO3 |