关于CuSO4溶液和Fe(OH)3胶体描述正确的是
| A.两者都能产生丁达尔现象 |
| B.两者都不能产生丁达尔现象 |
| C.CuSO4溶液能产生丁达尔现象,Fe(OH)3胶体不能产生丁达尔现象 |
| D.CuSO4溶液不能产生丁达尔现象,Fe(OH)3胶体能产生丁达尔现象 |
| A.胶体区别于其它分散系的本质特性是丁达尔现象 |
| B.利用半透膜可除去淀粉溶液中的少量NaCl |
| C.Fe(OH)3胶体带正电荷 |
| D.加入电解质,胶体能发生凝聚 |
下列事实与胶体性质无关的是
| A.在豆浆里加入盐卤做豆腐 |
| B.河流入海处易形成沙洲 |
| C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路 |
| D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是
| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
向氢氧化铝溶胶中滴加一种溶液,首先能使胶体凝聚而沉淀,继续滴加该溶液时,沉淀又逐渐消失。该溶液不可能是 ( )
| A.稀盐酸 | B.稀硫酸 | C.氨水 | D.氢氧化钠溶液 |
在实验室不慎手被玻璃划破,可用FeCl3溶液紧急止血,其主要原因可能是 ( )
| A.FeCl3溶液具有杀菌消毒作用 | B.FeCl3溶液能使血液凝聚 |
| C.FeCl3能产生Fe(OH)3沉淀堵住伤口 | D.FeCl3溶液能使血液发生化学变化 |
将磷肥生产中形成的副产物石膏()转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。

(1)本工艺中所用的原料除、
外,还需要等原料
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:
(3)过滤Ⅰ操作所得固体中,除外还含有(填化学式)等物质,该固体可用作生产水泥的原料。
(4)过滤Ⅰ操作所得滤液是溶液。检验滤液中含有
的方法是
(5)已知不同温度下在100
水中达到饱和时溶解的量如下表:
| 温度(℃) |
0 |
20 |
60 |
| 7.4 |
11.1 |
18.2 |
60℃时的饱和溶液591
冷却到0℃,可析出
晶体
(6)氯化钙结晶水合物()是目前常用的无机储热材料,选择的依据是
a 熔点较低(29℃熔化) b 能导电 c 能制冷 d 无毒
(7)上述工艺流程中体现绿色化学理念的是:。
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
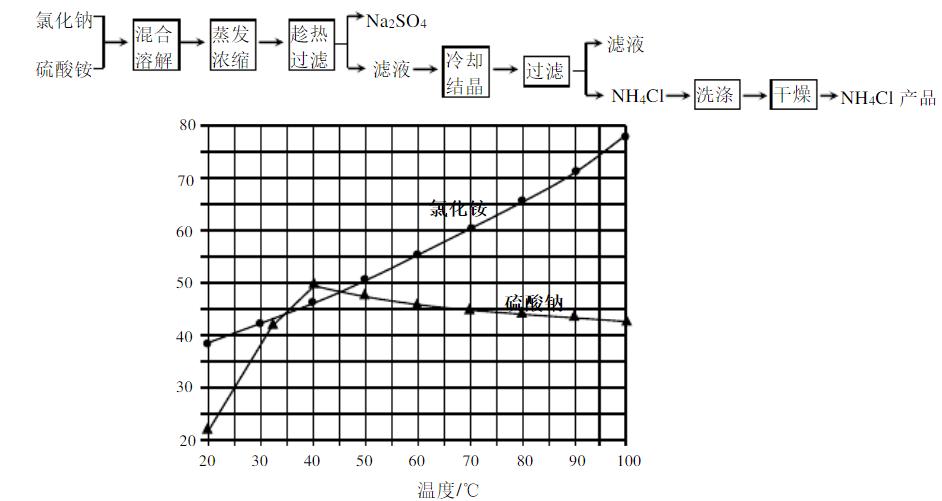
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7
,理论上需
。
(2)实验室进行蒸发浓缩用到的主要仪器有、烧杯、玻璃棒、酒精灯等。
(3)"冷却结晶"过程中,析出
晶体的合适温度为。
(4)不用其它试剂,检查
产品是否纯净的方法及操作是。
(5)若
产品中含有硫酸钠杂质,进一步提纯产品的方法是。
下列叙述正确的是( )
| A.直径介于1nm~100nm之间的微粒称为胶体 |
| B.电泳现象可证明胶体属电解质溶液 |
| C.利用丁达尔效应可以区别溶液与胶体 |
| D.胶体粒子很小,可以透过半透膜 |
“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将纳米材料分散到液体分散剂中,所得混合物可能具有的性质是(1纳米=10-9m)( )
| A.能全部透过半透膜 | B.有丁达尔现象 |
| C.所得液体一定是溶液 | D.所得物质一定是浊液 |
下列有关溶液性质的叙述,正确的是( )
| A.室温时饱和的二氧化碳水溶液,冷却到0℃时会放出一些二氧化碳气体 |
| B.20℃,100g水可溶解34.2g KCl,此时KCl 饱和溶液的质量分数为34.2% |
| C.强电解质在水中溶解度一定大于弱电解质 |
| D.相同温度下,把水面上的空气换成相同压力的纯氧,100g水中溶入氧气的质量增加 |
已知某盐在不同温度下的溶解度如下表.若把质量分数为22%的该盐溶液,由50℃逐渐冷却,则开始析出晶体的温度范围是( )
| 温度℃ |
0 |
10 |
20 |
30 |
40 |
| 溶解度(g/100g水) |
11.5 |
15.1 |
19.4 |
24.4 |
37.6 |
| A.0℃~10℃ | B.10℃~20℃ | C.20℃~30℃ | D.30℃~40℃ |