金属防腐是科学研究中的重大课题。某校学习小组以铁的腐蚀为项目进行如下研究。
[认识铁的腐蚀]
(1)下列环境中的铁制品最容易生锈的是 (填字母序号)。
A.未擦干的铁锅 B.涂油漆的栏杆 C.盛水的不锈钢水杯
(2)铁锈的主要成分是Fe2O3•xH2O,其中铁元素的化合价是 。
[探究铁的腐蚀]
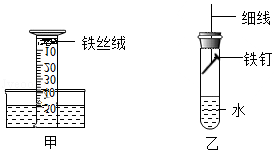
(3)该小组用如图甲装置进行实验,起始时量筒内水面处于50mL刻度处,之后水面缓慢上升。几天后水面最终处于约 (填“40”或“10”)mL刻度处,原因是 。
[拓展探究]
(4)小强同学进行如下实验:取铁钉用砂纸打磨,称其质量,按如图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
铁钉质量增加/g |
0.02 |
0.04 |
0.08 |
0.16 |
0.18 |
0.18 |
0.18 |
小强同学的实验是探究 因素对铁钉腐蚀快慢的影响,结论是 。
注意:若答对第(5)小题奖励3分,化学试卷总分不超过40分。
(5)有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因: ;改进实验方案证明你的分析: 。
氯化钯(PdCl2)可用于检测CO.PdCl2中Pd的化合价为( )
A.+1B.+2C.+3D.+4
小明在学习了元素和物质的知识后,进行了梳理,共中正确的是( )
A.铁元素的质量分数由高到低:FeO、Fe2O3、FeS
B.钙的化合物在水中的溶解性由大到小:CaCl2、CaCO3、Ca(OH)2
C.氮元素的化合价由高到低:HNO3、NH3、NO
D.空气中主要气体的体积分数由大到小:O2、N2、CO2
高氯酸钾(化学式为KClO4)是烟花中常用的氧化剂,可增加烟花的亮度。高氯酸钾中氯元素的化合价为( )
A.﹣7B.﹣1C.+5D.+7
我国研发的"碲化铋(Bi 2Te 3)纤维素复合热电薄膜电池",能利用人体热量为手表等可穿戴电子设备供电。
(1)纤维素的化学式为(C 6H 10O 5) n,这种物质属于 (选填"有机物"或"无机物")。
(2)Bi 2Te 3中碲(Te)元素的化合价为﹣2价,则Bi 2Te 3中铋(Bi)元素的化合价为 。
有一种在古籍里称为鋈的银白色铜合金,是古代云南、四川地区的特产,其主要成分是铜、锌、镍等金属单质。炼制时需要黑铜矿(主要成分是CuO)、硫化镍矿(主要成分是Ni2S3)等多种矿物。下列有关说法不正确的是( )
A.鋈属于金属材料
B.鋈的样品在足量稀盐酸中能全部溶解
C.Ni2S3的镍元素呈+3价
D.黑铜矿跟木炭共热能生成单质铜
对下列各组物质的判断错误的是( )
A.SO2与SO3﹣﹣组成元素相同
B.CO与N2﹣﹣相对分子质量相同
C.C2H4与C3H6﹣﹣碳元素质量分数相等
D.NaNO3与KMnO4﹣﹣氮元素与锰元素的化合价相同
已知4FeS2+11O2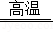 2Fe2O3+8X,则下列关于该反应说法错误的是( )
2Fe2O3+8X,则下列关于该反应说法错误的是( )
A.O2与X的相对分子质量之比为1:2
B.该反应属于置换反应
C.X属于空气污染物之一
D.该反应中硫元素的化合价升高
亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,超标会危害人体健康。亚硝酸钠和食盐外观很相似,容易误食导致中毒。已知亚硝酸钠溶液呈碱性。
(1)亚硝酸钠中N元素的化合价是 ;
(2)将酚酞试液分别滴加到亚硝酸钠和食盐溶液中,能使酚酞变红的是 溶液。
我国科学家研制出一种含镓元素(Ga)的催化剂一ZnGa2O4,在该催化剂表面成功将CO2转化为碳氢化合物燃料。下列关于ZnGa2O4的说法中,正确的是( )
A.其中Ga元素化合价为+3
B.由一种金属元素和两种非全属元素组成
C.锌、镓、氧元素的质量比为1:2:4
D.将CO2转化为碳氢化合物的过程中不需要添加其它物质
过氧化氢(H2O2)既是工业上重要的氧化剂,又是常用的医药消毒剂。
(1)H2O2中氧元素的化合价是 价,其中氢氧两种元素的质量比为 ,
(2)某过氧化氢的水溶液中,溶质与溶剂的质量比为1:4,该溶液中溶质的质量分数为 ,100克该溶液中氧元素质量为 克。(精确到0.1克)
请用化学用语回答下列问题。
(1)生活中常用氢气或氦气填充气球,但氢气球容易爆炸,氦气球则相对安全,应用较广。氦气的化学式为 。
(2)“喝酒不开车,开车不喝酒”。交警使用的酒精检测器里盛放经过酸化处理的含强氧化剂三氧化铬(CrO3)的硅胶,如果司机喝过酒,呼出气体中含有的乙醇蒸气将CrO3还原成硫酸铬[Cr2(SO4)3],检测器就会由暗红色变成蓝绿色。硫酸铬中铬元素的化合价为 。
(3)在许多金属矿物中含有一种非金属元素,在冶炼过程中该非金属元素会转化为大气污染物,该非金属元素的微粒结构示意图为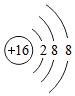 .请写出该微粒的符号: 。
.请写出该微粒的符号: 。
高铁酸钾(K2FeO4)可用于净水,也可用作电池的电极材料,可通过下列反应制备:
①MnO2+4HCl(浓)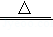 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②3Cl2+2Fe(OH)3+xKOH═2K2FeO4+6KCl+yH2O
下列说法正确的是( )
A.在反应①中,氯的化合价全部发生了改变
B.反应②中x=10,y=6
C.反应①②中共涉及了5种类型的化合物
D.上述反应不属于四种基本反应类型中的任何一种
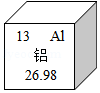
铝是生活中用途很广的金属材料。根据如图回答问题:
(1)铝原子核内的质子数为 。
(2)铝的相对原子质量为 。
(3)地壳中含量最多的元素与铝元素组成的化合物的化学式为 ,该化合物中铝元素的化合价为 。