碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。
[配制溶液]配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是 (填字母)。
a.用托盘天平称取2g Na2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 |
Ⅰ |
Ⅱ |
III |
溶质质量分数 |
1% |
2% |
4% |
溶液pH |
11.62 |
11.76 |
11.90 |
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是 。
[制备物质]用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是 (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:4FeCO3+6H2O+O2═4X+4CO2.则X的化学式为 。
[标定浓度]标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于lg•mL﹣1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将 (填“偏大”、“偏小”或“无影响”)。
某兴趣小组制取氧气,并尝试回收部分药品。可能用到的部分装置如图1。

(1)如图1中仪器a的名称是 。
(2)用双氧水和MnO2制氧气。发生反应的化学方程式为 ,收集氧气的装置可选用 (填字母)。
(3)加热KClO3固体制氧气(1.5g MnO2作催化剂),并对KClO3完全分解后的残留固体进行分离。(已知反应原理为:2KClO3 2KCl+3O2↑)
①发生装置应选用 (填字母)。
②KCl的溶解度曲线如图2所示。将残留固体冷却至室温(20℃),称得其质量为4.8g。欲将KCl全部溶解。至少应加入该温度下蒸馏水的体积约 (填字母)。

a.5mL
b.10mL
c.20mL
d.30mL
③对溶解所得混合物进行过滤,滤渣经处理得MnO2,从滤液中获得KCl晶体的最佳方法是 。
波尔多液含氢氧化钙、氢氧化铜和硫酸钙等物质,是农业上常用的杀菌剂。一种生产波尔多液的工艺流程如图。
(1)“煅烧”的化学方程式为CaCO3 CaO+CO2↑,该反应属于基本反应类型中的 反应。
(2)“混合”时不能用铁制容器,原因是 。
(3)“混合”时需不断搅拌,目的是 。
(4)“混合”过程中硫酸铜和氢氧化钙反应生成氢氧化铜的化学方程式为 。
(5)“混合”后得到的波尔多液温度明显高于室温,原因是 。
(6)用 可以测定波尔多液酸碱度。

研究气体的制备及相关气体的性质。
(1)写出实验室用过氧化氢溶液制取氧气的化学方程式 。
(2)写出实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式 。
(3)某同学为了便于加入液体药品,在如图装置的橡胶塞上添加了一个注射器,该同学发现,这样做的优点还有 (写出其中一点)。
(4)实验室里制取气体的一般思路和方法:
①选择适当的反应,包括 ;
②选择合适的 ;
③验证所制得的气体。
(5)请设计实验验证制得的氧气和二氧化碳气体,并完成实验报告。
实验步骤 |
实验现象 |
实验结论 |
|
|
|

下列图示实验操作正确的是( )
A. 测溶液pHB.
测溶液pHB. 倾倒液体
倾倒液体
C. 量筒读数D.
量筒读数D. 点燃酒精灯
点燃酒精灯
化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。
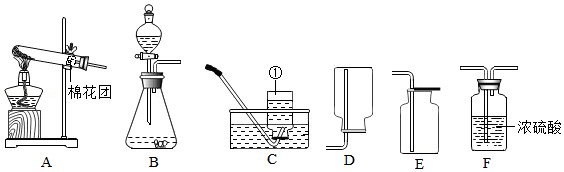
(1)图中标有序号①的仪器名称是 。
(2)实验室用A装置制取氧气,发生反应的化学方程式是 ,在试管口放棉花团的作用是 。
(3)用双氧水制取氧气,探究石蜡燃烧的产物,应选择装置B与 、 (填字母)组合。收集过程中,检验氧气集满的方法是 。
下列实验操作符合规范要求的是( )
A. 闻气体气味B.
闻气体气味B. 熄灭酒精灯
熄灭酒精灯
C. 稀释浓硫酸D.
稀释浓硫酸D. 给液体加热
给液体加热
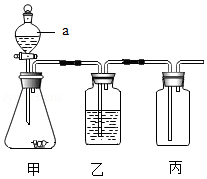
如图是初中化学常用实验装置(夹持装置已省略)。
(1)仪器a的名称是 。
(2)该装置用于实验室制取CO2:装置甲中发生反应的化学方程式为 。
(3)该装置用于实验室制取干燥的O2:乙中存放的试剂为 。检验丙中气体是否收集满的方法是 。
(4)该装置用于实验室制取干燥的H2:对装置所作的简单改动可以是 。
(5)该装置用于混合物中物质含量测定:在丙装置后连接量气装置,取10.0g黄铜(铜锌合金)粉末于锥形瓶中,加入足量稀硫酸,待完全反应后,根据气体体积换算得到生成的氢气质量为0.1g,则该混合物中铜的质量分数为多少?(写出计算过程)。
下列实验操作中,玻璃棒的作用与其它三个不同的是( )
A.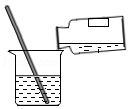 稀释B.
稀释B.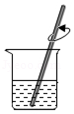 溶解
溶解
C.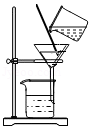 过滤D.
过滤D. 蒸发
蒸发
某工厂利用废铁屑与废硫酸反应制取绿矾(FeSO4•7H2O)。
(1)绿矾中铁原子与氧原子个数比为 。
(2)现有废硫酸4.9t(硫酸的质量分数为20%)与足量的废铁屑反应,理论上可生产出绿矾的质量是多少?(请写出计算过程,结果保留三位有效数字,下同)
(3)若配制100g质量分数为20%的稀硫酸溶液,需质量分数为98%的浓硫酸的体积是多少?(已知:质量分数为98%的浓硫酸的密度为1.84g/cm3)。
在实验室中,我们常用如图所示装置制取和收集某些气体。

(1)写出a、b两种仪器的名称。a ,b为 。
(2)实验室若用KMnO 4制取O 2,写出其化学方程式 ,相应的发生装置为 (填字母代号)。
(3)若选用装置C制备CO 2,则可以选择 (填字母代号)。
a.块状碳酸钙和稀盐酸
b.块状碳酸钙和稀硫酸
(4)经查阅资料,Na 2O 2(过氧化钠)也能与水迅速反应产生O 2.补全下列反应方程式:2Na 2O 2+2H 2O═
(5)收集O 2适合选用 装置(填字母代号)。
a.仅D
b.仅E
c.D和E