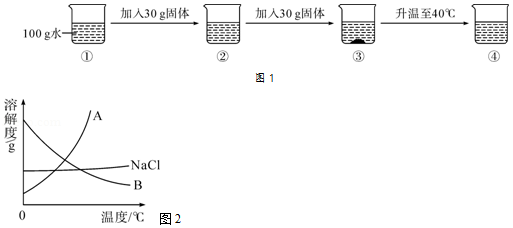
20℃时,某固体物质的溶解度为40g。该温度下,向盛有100g水的烧杯中,分两次各加入30g该固体,充分搅拌后,再升高温度至40℃,实验过程如图1所示:
请回答下列问题:
(1)20℃时,②中烧杯内溶液为 (填"饱和"或"不饱和")溶液。
(2)根据如图实验判断该固体物质的溶解度曲线应为图2中的曲线 (填"A"或"B")。
(3)③中烧杯内固体的质量是 g。
(4)若该固体中混有少量NaCl杂质,提纯时,可采用 的方法。
20℃时,某固体物质的溶解度为40g。该温度下,向盛有100g水的烧杯中,分两次各加入30g该固体,充分搅拌后,再升高温度至40℃,实验过程如图1所示:

请回答下列问题:
(1)20℃时,②中烧杯内溶液为 (填"饱和"或"不饱和")溶液。
(2)根据如图实验判断该固体物质的溶解度曲线应为图2中的曲线 (填"A"或"B")。
(3)③中烧杯内固体的质量是 g。
(4)若该固体中混有少量NaCl杂质,提纯时,可采用 的方法。