本题有两部分
I:软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4·H2O,反应的化学方程式为:MnO2+SO2=MnSO4
(1)质量为17.4g纯净MnO2最多能氧化____________L(标准状况)SO2。
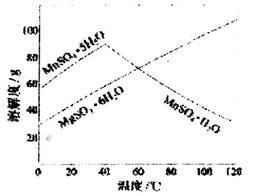
(2)上述反应制得的溶液,调节pH值到5~7的范围,以除去Fe3+、 Al3+(使其浓度小于l×10-6mol·L-1),然后从得到的MnSO4和 MgSO4混合溶液中结晶MnSO4·H2O晶体,下图可以看出,需控制结晶温度在_______以上。
II:以磷石膏(主要成分CaSO4,杂质SiO2、A12O3等)为原料可制备轻质CaCO3。

(1)匀速向浆料中通入CO2,浆料清液的pH和c(SO42-)随时间变化见下图。清液pH>11时CaSO4转化的离子方程式_______________________

(2)当清液pH接近6.5时,过滤并洗涤固体。滤液中物质的量浓度最大的两种阴离子为SO42-和_______(填化学式);检验洗涤是否完全的方法是____________。
(3)磷石膏若用氢氧化钠溶液溶解,发生反应的有关离子方程式为:
_________________________________ 、____________________________________
 2CH3COOH。
2CH3COOH。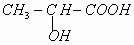 。
。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号