汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)已知:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂)
2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂)
2C (s)+O2(g) 2CO(g)△H=-221.0KJ/mol
2CO(g)△H=-221.0KJ/mol
C (s)+O2(g) CO2(g)△H=-393.5KJ/mol
CO2(g)△H=-393.5KJ/mol
则N2(g)+O2(g)=2NO(g)△H= kJ·mol-1。
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s
|
0
|
1
|
2
|
3
|
4
|
5
|
C(NO)10-4 mol/L
|
10.0
|
4.50
|
C1
|
1.50
|
1.00
|
1.00
|
C(CO)10-3 mol/L
|
3.60
|
3.05
|
C2
|
2.75
|
2.70
|
2.70
|
则c1合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.3.50 D.2.50
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率。根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如下图所示:
实验
编号
|
T/°C
|
NO初始浓
度/10-3mol•L-1
|
CO初始浓
度/10-3mol•L-1
|
催化剂的比
表面积/m2•g-1
|
①
|
350
|
1.20
|
5.80
|
124
|
②
|
280
|
1.20
|
5.80
|
124
|
③
|
280
|
1.20
|
5.80
|
82
|
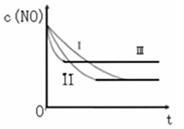
则曲线I对应的实验编号为 。
(4)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
|
温度/℃
|
起始量/mol
|
平衡量/mol
|
达到平衡所
需时间/min
|
H2O
|
CO
|
CO
|
H2
|
①
|
650
|
2
|
4
|
2.4
|
1.6
|
5
|
②
|
900
|
1
|
2
|
1.6
|
0.4
|
3
|
③
|
900
|
a
|
b
|
c
|
d
|
t
|
①实验组①中以v(CO2)表示的反应速率为 。
②若a=2,b=1,则c= ,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为:α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。
①则负极的电极反应式为________________。
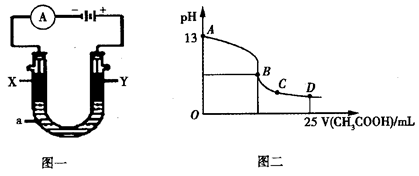
②以上述电池为电源,通过导线连接成图一。若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式 。电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图二计算,上述电解过程中消耗一氧化碳的质量为__________g。
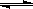 2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下: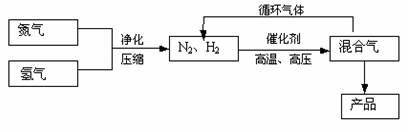
 2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂)
2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂) CO2(g)△H=-393.5KJ/mol
CO2(g)△H=-393.5KJ/mol

 粤公网安备 44130202000953号
粤公网安备 44130202000953号