某种硬铝合金是由 Al、Cu、Mg三种金属组成,主要应用于耐热可焊的结构件及锻件。某研究小组欲探究该合金的性质并测定合金中铝的质量分数:
(1)甲同学预测:该合金与10 mol/L硝酸反应时有NO2气体生成,可能还有NO生成。
查阅资料:常温下,NO2与N2O4混合存在,在低于0 ℃时几乎只有无色的N2O4液体或晶体存在。
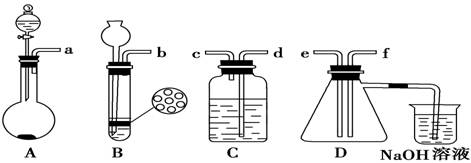
设计如下装置进行实验。按下图连接装置并检验气密性后,称取5 g 合金放于圆底烧瓶中,并滴加10 mol/L硝酸。
①合金中Cu与稀硝酸反应的离子方程式是 。
②C装置的目的是 。
③能证明有NO2生成的实验现象是 ,能证明有NO生成的实验操作与现象是 。
④实验进行至A中固体全部溶解后,未检验到有NO生成,甲同学认为硬铝合金与10 mol/L硝酸反应时没有NO生成。乙同学认为不能确定是否生成了NO,需补充操作才能证明,该操作是 。
(2)为测定合金中铝的质量分数,丙同学查阅资料:
部分金属离子生成氢氧化物沉淀的pH
| 金属离子 |
开始沉淀时的pH |
沉淀完全的pH |
| Al3+ |
3.4 |
4.7 |
| Cu2+ |
4.1 |
6.9 |
| Mg2+ |
9.4 |
12.4 |
pH > 7.8时,Al(OH)3开始溶解,pH > 10.8时沉淀完全溶解。
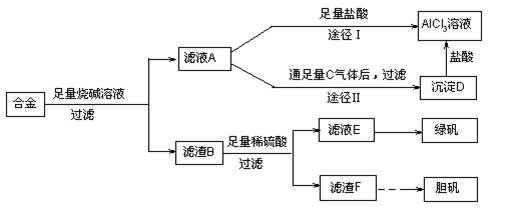
设计如下方案并进行实验:
①调节pH时,应控制pH的范围是 。
②选用NaOH溶液调节pH,得到溶液B的离子方程式是 。
③Al(OH)3经过滤、洗涤、灼烧至恒重后称量,质量为8.5g,则该合金中铝的质量分数是 。
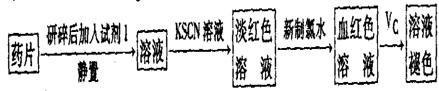
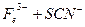
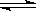
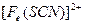 。
。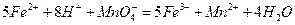 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。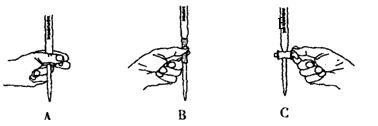
 粤公网安备 44130202000953号
粤公网安备 44130202000953号