【改编】(15分)ClO2气体是一种常用的消毒剂,依据该反应制得
2KClO3+H2C2O4+2H2SO4 2ClO2↑+2CO2↑+2KHSO4+2H2O。
2ClO2↑+2CO2↑+2KHSO4+2H2O。
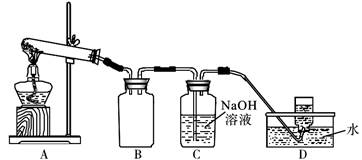
I、已知:二氧化氯(ClO2)的熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。某学生拟用下图所示装置模拟工业制取及收集ClO2。(夹持仪器已省略)。回答下列问题:

(1)B必须添加温度控制装置,应补充的装置是__________________。
(2)C装置中反应后生成的主要物质是Na2CO3、NaClO2、和___________。
(3)消毒水时,ClO2还可将Fe2+、Mn2+转化成Fe(OH)3、MnO2难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明C1O2具有________________性。
II、为测定所得溶液中ClO2的含量,进行下列实验:准确量取ClO2溶液10 mL,稀释成100 mL试样;量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,反应原理:2ClO2+10I-+8H+=2Cl-+5I2+4H2O, 2Na2S2O3 + I2 =Na2S4O6 + 2 NaI,消耗Na2S2O3溶液V2 mL。
(4)滴定过程中至少须进行两次平行测定的原因是__________________________________。
(5)原ClO2溶液的浓度为____________g/L(用含字母的代数式表示)。

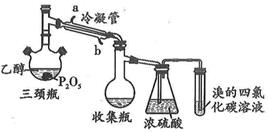
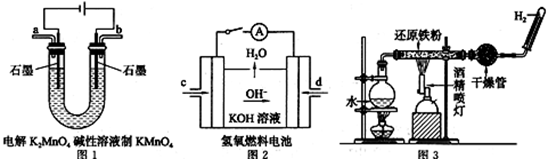
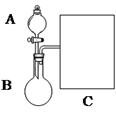

 )工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。
)工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。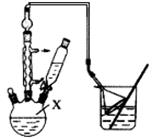
 粤公网安备 44130202000953号
粤公网安备 44130202000953号