碱金属元素的单质和化合物在日常生活和化工生产中应用广泛。
(1)钠的原子结构示意图为______________________。
(2)过氧化钠可作为呼吸面具和潜水艇中的供氧剂。写出过氧化钠与二氧化碳反应的化学方程式:___。
(3)氯碱工业是利用电解饱和食盐水获取一系列化工产品的过程。若利用电解饱和食盐水所得的气体制100t 36.5%的浓盐酸,理论上至少需要消耗NaCl_________________ t。
(4)某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
①分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A的名称为_______。
②称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL 蒸馏水,振荡,发现Na2CO3固体完全溶解,而NaHCO3固体还有剩余,由此可以得出结论:___________。向所得溶液中滴入酚酞后,观察到的现象是________________。
③某同学为探究Na2CO3和NaHCO3与CaCl2溶液的反应,将两种固体分别配制成0.5 mol/L的溶液,设计如下方案并对反应现象做出预测:
| 实验方案 |
预测现象 |
预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1 mL 0.5 mol/L CaCl2溶液 |
有白色沉淀 |
Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应Ca2+ + CO32-=" " CaCO3↓。 |
| 操作2:向2mL NaHCO3溶液中滴加1 mL 0.5 mol/L CaCl2溶液 |
无白色沉淀 |
NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应。 |
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体。则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为:___________________________。
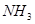 和
和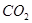 是两种重要的化工原料。
是两种重要的化工原料。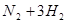

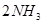 。该可逆反应达到化学平衡的标志是___________(填字母)。
。该可逆反应达到化学平衡的标志是___________(填字母)。
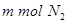 的同时消耗
的同时消耗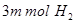
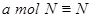 键断裂的同时,有
键断裂的同时,有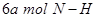 键断裂
键断裂 △
△
 △
△ ,则2mol二氧化碳完全反应合成尿素的△H=_______。
,则2mol二氧化碳完全反应合成尿素的△H=_______。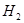 体积比为1:4时反应,
体积比为1:4时反应,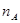 、
、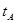 、V表示)。
、V表示)。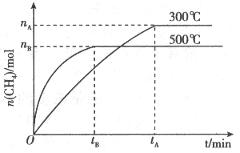
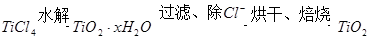
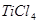 水解生成
水解生成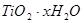 的化学方程式是_________;检验
的化学方程式是_________;检验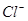 是否被除净的方法是_________。
是否被除净的方法是_________。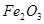 的钛铁矿(主要成分为
的钛铁矿(主要成分为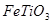 ,其中
,其中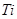 化合价为+4价)制取,其主要流程如下:
化合价为+4价)制取,其主要流程如下: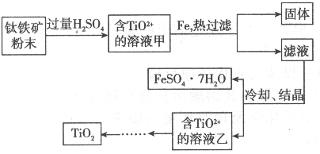
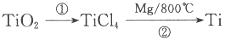
 的气氛中进行,原因是________________。
的气氛中进行,原因是________________。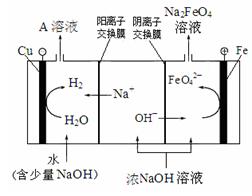
 CH3OH(g) △H="a" kJ/mol
CH3OH(g) △H="a" kJ/mol )及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
)及温度的关系,研究小组在10 L的密闭容器中进行模拟反应,并绘出下图:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号