附加题某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下所示(写出最佳答案)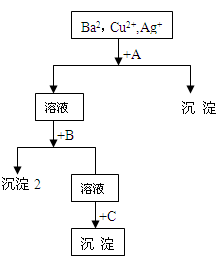
(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式: 。溶液+B的离子方程式: 。
附加题某溶液中含有Ba2+,Cu2+, Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下所示(写出最佳答案)
(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式: 。溶液+B的离子方程式: 。