磺化煤(表达式为NaR)是一种钠离子型离子交换剂,它能与硬水中的Ca2+、Mg2+交换而将其除去,从而使水软化。现代海水的淡化方法是使海水按顺序通过两种离子交换剂,其流程如图所示。
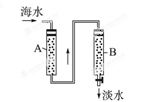
(1)现有氢型阳离子交换树脂(HR)和羟型阴离子交换树脂(ROH),则在图中的离子交换柱中应分别装入的离子交换树脂是(填表示式):A柱为______ ______,B柱为____________。
(2)说明上述顺序的理由_______________________________________________。