某学生做淀粉水解实验,步骤如下: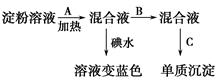
(1)写出淀粉水解的化学反应方程式_______。
(2)单质沉淀是________________(写化学式)。
(3)填写所加试剂名称及其作用:
A.____________,作用_______________________;
B.____________,作用_____________________。
某学生做淀粉水解实验,步骤如下:
(1)写出淀粉水解的化学反应方程式_______。
(2)单质沉淀是________________(写化学式)。
(3)填写所加试剂名称及其作用:
A.____________,作用_______________________;
B.____________,作用_____________________。