已知A—H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据右图所示的转化关系(图中反应条件均已略去),请回答: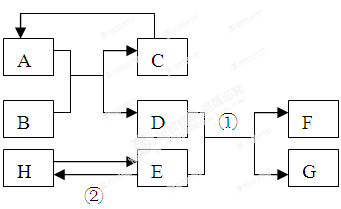
(1)写出下列物质的化学式:B 、C ;
(2)写出下列反应的化学方程式:① ;
② ,反应②的基本反应类型是 。
已知A—H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据右图所示的转化关系(图中反应条件均已略去),请回答:
(1)写出下列物质的化学式:B 、C ;
(2)写出下列反应的化学方程式:① ;
② ,反应②的基本反应类型是 。