由钛铁矿(主要成分是FeO和TiO2的混合物)提取金属钛(化学式为Ti)的主要工艺流程如下: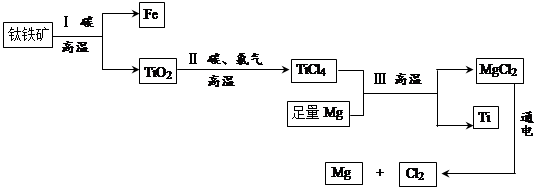
(1)上述流程中的物质属于氧化物的是 (填一种化学式即可),属于非金属单质的是 (填一种化学式即可),TiO2中钛元素的化合价是 。
(2)步骤Ⅰ中FeO和碳反应生成二氧化碳和铁,反应的符号表达式是 。
(3)该流程中可循环利用的物质是 。
由钛铁矿(主要成分是FeO和TiO2的混合物)提取金属钛(化学式为Ti)的主要工艺流程如下:
(1)上述流程中的物质属于氧化物的是 (填一种化学式即可),属于非金属单质的是 (填一种化学式即可),TiO2中钛元素的化合价是 。
(2)步骤Ⅰ中FeO和碳反应生成二氧化碳和铁,反应的符号表达式是 。
(3)该流程中可循环利用的物质是 。