某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:常温下将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1 mL,分别加水稀释到1 000 mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题: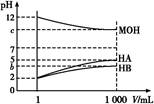
(1)HA为 酸,HB为 酸(填“强”或“弱”)。
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为 (用酸、碱化学式表示)。
(3)若c=9,将稀释后的HA溶液和MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为c(A-) (填“大于”、“小于”或“等于”)c(M+)。
(4)若b+c=14,则MOH为 碱(填“强”或“弱”)。将稀释后的HB溶液和MOH溶液取等体积混合,所得混合溶液的pH 7(填“大于”、“小于”或“等于”)。
 CO(g) ΔH="-110.5" kJ·mol-1②Mg(g)+O2(g)
CO(g) ΔH="-110.5" kJ·mol-1②Mg(g)+O2(g) Mg(g)+CO(g),该反应的ΔH= 。
Mg(g)+CO(g),该反应的ΔH= 。



 )
) 粤公网安备 44130202000953号
粤公网安备 44130202000953号