用18 mol/L 的浓硫酸配制100 mL 3.0 mol/L 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解
④检漏、转移、洗涤 ⑤定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (用下列编号填空)。
| A.10ml | B.25ml | C.50ml | D.100ml |
(2)第③步实验的操是 。
(3)第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线 ;改用 向容量瓶中滴加蒸馏水至 为止。塞紧瓶塞,倒转摇匀并装试剂瓶。
(4)转移溶液和直接加蒸馏水于容量瓶中要注意“两靠”:一靠是盛溶液的烧杯口靠在玻璃棒上部,二靠是玻璃棒下端靠在 。
(5)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”、“偏小”、“无影响”填写)
①容量瓶用蒸馏水洗涤后残留有少量的水 ;
②所用过的烧杯、玻璃棒未洗涤 ;
③加水超过刻度线后,用胶头滴管吸出多余的液体 。


 +2H+ =Fe3++NO2↑+H2O
+2H+ =Fe3++NO2↑+H2O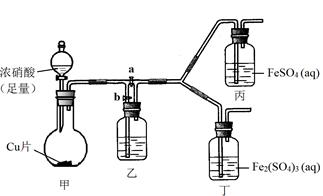

 粤公网安备 44130202000953号
粤公网安备 44130202000953号