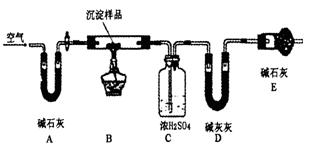
(6分)如图为实验室制取蒸馏水的装置示意图,根据下图回答下列问题。
(1)指出图中的两处明显的错误:
_____________________________;_____________________________ 。
(2)水在 a中(填仪器的名称,下同)由液态变为气态,在 b中由气态变为液态。
(3)实验时A中除加入少量自来水外,还需加入少量_____________,其作用是________________________________ 。
 61
61 程式是。
程式是。 某学生设计回收四氯化碳的操作步骤为:
某学生设计回收四氯化碳的操作步骤为:


 的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。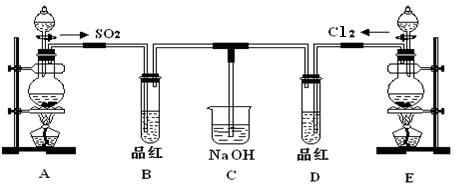
 MnCl2+Cl2 +2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:
MnCl2+Cl2 +2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质: 粤公网安备 44130202000953号
粤公网安备 44130202000953号