探究酸、碱和盐的性质及应用.
(1)NaOH溶液和稀硫酸反应,向滴有酚酞的NaOH溶液中加入稀硫酸,现象为 ,反应的化学方程式为 .
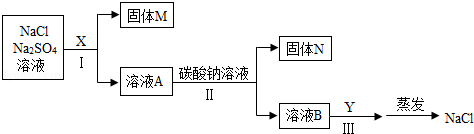
(2)为除去NaCl中混有的少量Na2SO4,某探究小组设计了如图所示方案进行实验.
①Ⅰ、Ⅱ两步都有过滤操作,过滤中要用到的玻璃仪器有 .
②甲、乙同学选用的X分别为BaCl2溶液、Ba(OH)2溶液,写出Ⅰ、Ⅱ两步中发生的任意一个反应的化学方程式 ,甲、乙同学的实验中,可能发生的相同反应的化学方程式为 ,乙的实验中,步骤Ⅲ涉及的操作和现象是 .
③丙同学认为甲的实验比乙的实验更合理,理由是 .